Microbiote et maladies chroniques : ce que la science commence à comprendre
Covid long, fibromyalgie, syndrome de fatigue chronique — trois diagnostics différents, souvent sans solution claire, qui touchent majoritairement les femmes entre 35 et 55 ans. Une piste commune émerge dans la littérature scientifique récente : la perturbation du microbiote intestinal, de la barrière intestinale et de l'axe qui relie l'intestin au cerveau. Voici ce que les données montrent, et ce qu'elles ne permettent pas encore de conclure.
⚡ L'essentiel en 4 points
Un fil commun
Covid long, fibromyalgie et ME/CFS partagent des altérations du microbiote intestinal : moins de diversité, moins de bactéries productrices de butyrate.
L'axe gut-brain
L'intestin et le cerveau communiquent via le nerf vague, les métabolites microbiens et le système immunitaire. Une dysbiose perturbe cette communication.
Association, pas causalité
Les études sont observationnelles : la dysbiose est associée à ces conditions, mais son rôle causal n'est pas encore formellement démontré.
Pistes thérapeutiques
Probiotiques, alimentation riche en fibres et transplantation de microbiote fécal sont en cours d'évaluation — mais aucune recommandation clinique standardisée n'existe encore.
📖 Termes de référence
- Dysbiose = Gut dysbiosis — déséquilibre de la composition du microbiote intestinal
- Axe gut-brain (axe intestin-cerveau) = Gut-brain axis — réseau de communication bidirectionnel entre intestin et cerveau
- Butyrate = Butyrate — acide gras à chaîne courte (AGCC) produit par certaines bactéries intestinales, à effets anti-inflammatoires
- Faecalibacterium prausnitzii = principal producteur de butyrate de l'intestin humain sain
- Tryptophane = Tryptophan — acide aminé précurseur de la sérotonine, dont le métabolisme est altéré en cas de dysbiose
- Kynurénine = Kynurenine — voie métabolique alternative du tryptophane, pro-inflammatoire, activée en cas de dysbiose
- PASC = Post-Acute Sequelae of SARS-CoV-2 — terme scientifique pour le Covid long
- ME/CFS = Myalgic Encephalomyelitis / Chronic Fatigue Syndrome — encéphalomyélite myalgique / syndrome de fatigue chronique
- LPS = Lipopolysaccharide — fragment bactérien qui traverse une barrière intestinale perméable et active le système immunitaire systémique
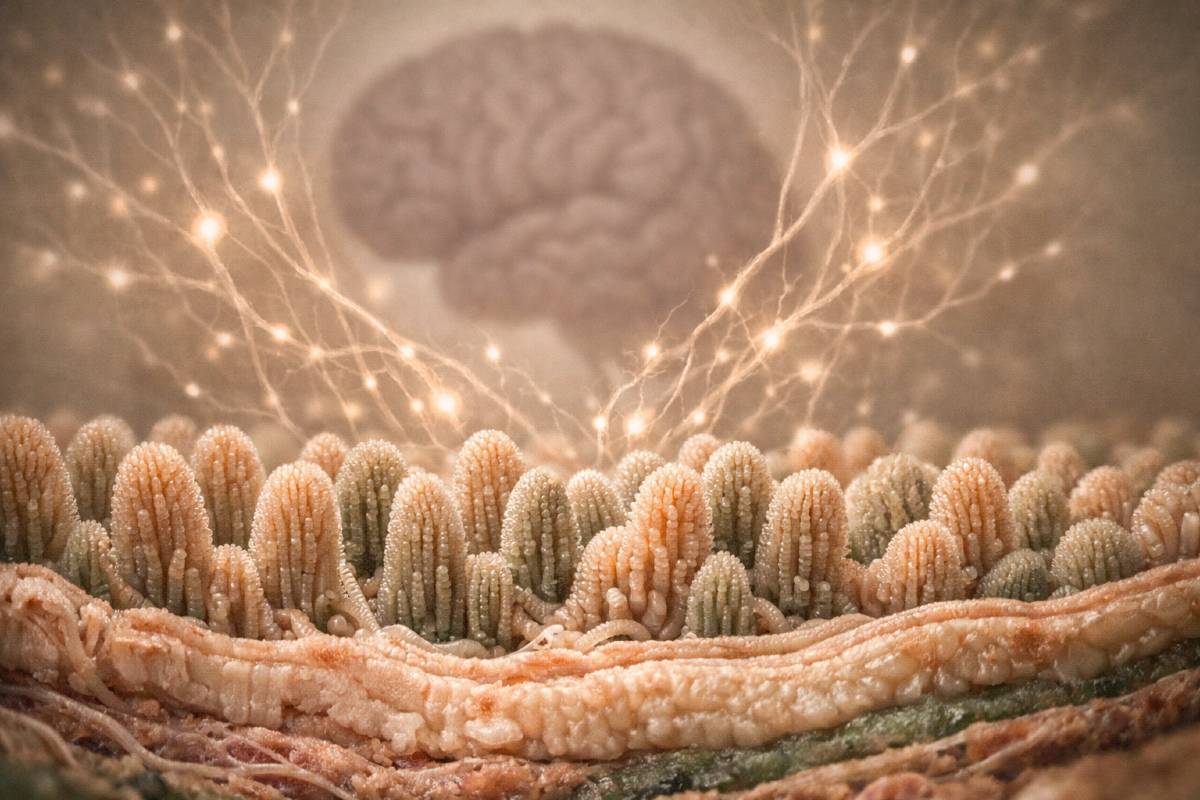
Trois maladies, un fil invisible
🟠 Convergence observationnelle — revues systématiques 2025Fibromyalgie, syndrome de fatigue chronique (ME/CFS), Covid long : trois conditions qui partagent un profil clinique déconcertant. Fatigue invalidante, douleurs diffuses, brouillard cognitif, troubles du sommeil — et souvent, des examens biologiques standards qui reviennent dans les normes. Elles touchent majoritairement les femmes, surviennent fréquemment après un épisode infectieux ou un stress intense, et résistent aux approches thérapeutiques conventionnelles.
Ce qu'on commence à mieux comprendre, c'est qu'elles partagent aussi des mécanismes biologiques. Au centre de cette convergence : un microbiote intestinal perturbé, une barrière intestinale fragilisée, et un axe de communication gut-brain qui s'emballe. Une revue narrative publiée en 2025 dans International Journal of Molecular Sciences les regroupe explicitement sous le concept d'« environmental sensitivity illnesses » avec des mécanismes communs : déplétion des taxa anti-inflammatoires, enrichissement des espèces pro-inflammatoires, altération des acides gras à chaîne courte, dysfonction mitochondriale et neuroinflammation.[1]
⚠️ Ces données sont observationnelles. Elles décrivent des associations, pas des relations causales établies. La dysbiose est-elle une cause ou une conséquence de ces maladies ? La question reste ouverte dans la majorité des cas.
Les trois conditions convergent vers des perturbations biologiques communes autour de l'axe intestin-cerveau. Les flèches indiquent des associations, pas des relations causales établies.
Le microbiote intestinal : chef d'orchestre méconnu
🟢 Preuve établie — Consensus microbiologie humaineLe microbiote intestinal représente environ 100 000 milliards de micro-organismes qui colonisent notre tube digestif. Ces bactéries, virus et champignons ne sont pas de simples passagers : ils participent activement à la digestion, à la synthèse de vitamines, à la maturation du système immunitaire, et à la production de métabolites qui influencent directement le cerveau.
Un microbiote en bonne santé se caractérise par une haute diversité et un équilibre entre espèces pro- et anti-inflammatoires. Les bactéries productrices d'acides gras à chaîne courte (AGCC) — notamment le butyrate — occupent une place centrale. Elles nourrissent les cellules de la paroi intestinale, maintiennent l'intégrité de la barrière, et exercent des effets anti-inflammatoires à distance. Faecalibacterium prausnitzii est l'un des producteurs les plus étudiés.
Quand cet équilibre se rompt — on parle de dysbiose — les conséquences dépassent largement la sphère digestive. La barrière intestinale se fragilise, des fragments bactériens (LPS) passent dans la circulation générale, le système immunitaire s'active de façon chronique, et les voies métaboliques en dépendant se dérèglent.
L'axe gut-brain : quand l'intestin parle au cerveau
🟢 Preuve établie — Revues systématiques, physiologieL'intestin et le cerveau communiquent en permanence via un réseau complexe et bidirectionnel : le nerf vague (voie vagale directe), le système immunitaire, les hormones, et les métabolites produits par le microbiote. Cette communication est tellement dense que l'intestin est parfois appelé « second cerveau ».
L'axe gut-brain repose sur 4 voies simultanées. En cas de dysbiose, chacune d'elles peut transmettre des signaux pro-inflammatoires ou pro-douloureux vers le cerveau.
En cas de dysbiose, plusieurs dérèglements peuvent s'enchaîner. La barrière intestinale devient perméable : des fragments bactériens (LPS) franchissent la muqueuse et activent le système immunitaire de façon chronique. La production de butyrate diminue, réduisant la protection de la muqueuse et l'effet anti-inflammatoire systémique. Le métabolisme du tryptophane est dévié vers la voie kynurénine pro-inflammatoire au détriment de la sérotonine. Ces signaux perturbent la neuroinflammation, la perception de la douleur, et les fonctions cognitives.
ME/CFS : quand les bactéries productrices d'énergie disparaissent
🟠 Association documentée — Cohorte n=197, métagénomique (Columbia, 2023)C'est dans le ME/CFS que les données microbiote-maladie chronique sont aujourd'hui les plus solides. Une étude multicentrique publiée en 2023 dans Cell Host & Microbe (Guo et al., Columbia University) a analysé le microbiome de 106 personnes atteintes de ME/CFS et 91 contrôles sains par métagénomique shotgun couplée à la métabolomique.[2]
Résultat principal : Faecalibacterium prausnitzii et Eubacterium rectale, deux producteurs majeurs de butyrate dans l'intestin humain sain, sont significativement réduits dans le ME/CFS. La capacité de synthèse du butyrate est fonctionnellement déficiente — confirmée par métagénomique, PCR quantitative et mesure directe des acides gras fécaux. L'abondance de F. prausnitzii est inversement corrélée à la sévérité de la fatigue : plus elle est basse, plus la fatigue est intense.
Le modèle de classification basé sur le microbiome était robuste géographiquement et validé dans une cohorte externe — ce qui renforce la crédibilité du signal. Il ne s'agit pas d'une simple fluctuation liée au mode de vie.
Une revue publiée dans International Journal of Molecular Sciences (Nikolova et al., 2025) synthétise les mécanismes proposés : dysbiose → perméabilité intestinale accrue → translocation bactérienne → inflammation systémique → neuroinflammation → fatigue et brouillard cognitif. Les perturbations du métabolisme du tryptophane et l'acidose D-lactique sont identifiées comme pistes mécanistiques supplémentaires.[3]
Fibromyalgie : douleur, intestin et détresse psychologique
🟠 Association documentée — Revue systématique 10 études (2026)Dans la fibromyalgie, le signal est cohérent mais plus hétérogène. Une revue systématique publiée en 2026 dans Biopsychosocial Science and Medicine (Lanzara et al.) a analysé 10 études (7 cas-contrôles, 2 RCT, 1 observationnel).[4] Résultat : dysbiose et hyperperméabilité intestinale sont associées à une détresse émotionnelle, cognitive et somatique plus élevée chez les personnes fibromyalgiques.
Ce lien s'explique mécanistiquement. La fibromyalgie repose sur un mécanisme de sensibilisation centrale : le système nerveux amplifie les signaux douloureux de façon généralisée.[5] Or, les signaux inflammatoires issus d'un intestin perméable peuvent activer les cellules microgliales du cerveau et de la moelle épinière — contribuant à maintenir cette sensibilisation. L'axe gut-brain devient un amplificateur de douleur.
Une revue critique publiée en 2025 dans Clinical and Experimental Rheumatology (Shtrozberg et al.) confirme l'hypothèse mais souligne ses limites : effectifs faibles, cohortes hétérogènes, pas de biomarqueur reproductible, pas de recommandation clinique standardisée.[6] On ne peut pas conclure solidement que la correction du microbiote guérit la fibromyalgie.
👁️ L'œil du Docteur en pharmacie — Fibromyalgie et Covid long : convergence mécanistique
Ces deux conditions partagent des mécanismes biologiques remarquablement similaires : sensibilisation centrale, activation prolongée des cellules microgliales, perturbation de l'axe HPA, et parfois atteinte des petites fibres nerveuses. Ce n'est pas un hasard si une partie des personnes ayant développé un Covid long présente un tableau clinique proche de la fibromyalgie.
Le point de convergence microbiote est particulièrement intéressant : dans les deux conditions, on retrouve une déplétion des bactéries productrices de butyrate et une activation inflammatoire chronique de bas grade. Ce n'est pas une identité de maladie — mais une identité de mécanisme, ce qui ouvre la voie à des approches communes (soutien du microbiote, alimentation anti-inflammatoire, gestion du stress biologique) qui méritent d'être explorées avec un professionnel de santé formé à ces questions.
Pour approfondir les mécanismes spécifiques à la fibromyalgie : notre article dédié →
Covid long : dysbiose, inflammation et symptômes persistants
🟠 Association documentée — Revues systématiques + cohorte Nature Immunology (2024)Dans le Covid long, le lien microbiote-maladie est parmi les mieux documentés des trois conditions. Les personnes avec PASC présentent de façon consistante une déplétion en bactéries productrices d'AGCC (Faecalibacterium, Bifidobacterium), un enrichissement en espèces pro-inflammatoires, et des altérations de la barrière intestinale.[7]
Une cohorte de 657 personnes post-hospitalisation, publiée dans Nature Immunology en 2024 (Liew et al.), identifie des sous-types mécanistiques du Covid long : activation du complément, inflammation myéloïde, et perturbation de l'axe gut-brain — le marqueur SCG3 étant élevé dans les symptômes gastro-intestinaux.[8] Ces données plaident pour une hétérogénéité biologique du Covid long, avec des sous-groupes aux mécanismes distincts.
Dans notre article sur les piliers mécanistiques du Covid long, le Pilier 4 est précisément l'axe intestin-cerveau : dysbiose → perméabilité → translocation bactérienne → activation immunitaire → perturbation du métabolisme du tryptophane (sérotonine ↓, kynurénine ↑) → répercussions sur l'humeur, le sommeil et la cognition.
La cascade dysbiose → neuroinflammation → symptômes est mécanistiquement plausible et cohérente avec les données observationnelles. Elle n'est pas encore prouvée comme relation causale directe chez l'humain.
Ce que ça change — et ce que ça ne change pas encore
🔴 Signal préliminaire — Essais interventionnels de petite tailleProbiotiques : des essais préliminaires existent dans les trois pathologies. Les résultats sont encourageants sur la fatigue et les symptômes digestifs, mais les études sont souvent courtes, avec de petits effectifs et sans groupe contrôle robuste. On ne peut pas faire de recommandation clinique précise à ce stade. En parler à votre professionnel de santé avant de commencer une supplémentation est indispensable.
Alimentation : les régimes riches en fibres fermentescibles (prébiotiques) favorisent la production d'AGCC. Le régime méditerranéen est associé à une plus grande diversité microbienne. Mais « changer son alimentation guérit le Covid long » serait une extrapolation abusive — aucune étude interventionnelle humaine de grande taille ne l'a démontré.
Transplantation de microbiote fécal (TMF) : des essais sont en cours dans le ME/CFS et le Covid long. Les résultats préliminaires sont intéressants, mais la TMF reste expérimentale pour ces indications. Elle n'est pas disponible en routine en France pour ces pathologies.
Ce qui ne change pas : un microbiote perturbé n'est pas la seule explication de ces maladies. D'autres mécanismes coexistent — dysautonomie, réactivation virale, dysfonction immunitaire, dysfonction mitochondriale, neuropathie des petites fibres. Le microbiote est une pièce du puzzle, pas la pièce.
🧩 Ce que l'on sait — et ce que l'on ne sait pas encore
Ce qui est établi : Des altérations du microbiote intestinal sont observées de façon reproductible dans ME/CFS, fibromyalgie et Covid long. La déplétion en F. prausnitzii est inversement corrélée à la sévérité de la fatigue dans ME/CFS (Guo et al., 2023, cohorte géographiquement diversifiée). L'axe gut-brain est perturbé dans ces trois conditions, avec des mécanismes convergents (AGCC, tryptophane, perméabilité intestinale).
Ce qui reste spéculatif ou à confirmer : Le rôle causal de la dysbiose (cause ou conséquence ?). L'efficacité clinique des interventions probiotiques dans ces indications. L'existence de profils microbiens biomarqueurs fiables et reproductibles. La transposabilité des interventions d'une condition à l'autre malgré les mécanismes communs.
Questions fréquentes
Le microbiote intestinal peut-il vraiment influencer la fibromyalgie ?
Des études observationnelles montrent des altérations systématiques du microbiote chez les personnes atteintes de fibromyalgie, associées à une hyperperméabilité intestinale et une détresse psychologique plus élevée. Le lien causal reste à démontrer, mais la cohérence mécanistique est soutenue par plusieurs revues récentes. Il ne s'agit pas d'une cause unique, mais d'un amplificateur potentiel.
Quelle différence entre dysbiose et microbiote sain ?
Un microbiote sain est caractérisé par une haute diversité et un équilibre entre espèces pro- et anti-inflammatoires. La dysbiose désigne un déséquilibre : baisse de diversité, réduction des bactéries productrices de butyrate (Faecalibacterium, Bifidobacterium), augmentation des espèces opportunistes pro-inflammatoires. Ce n'est pas un état binaire mais un spectre.
Les probiotiques peuvent-ils aider dans le Covid long ?
Des études préliminaires suggèrent une amélioration de certains symptômes (fatigue, troubles digestifs, cognition) avec des probiotiques ou synbiotiques ciblés. L'évidence reste hétérogène et les essais contrôlés de grande taille manquent. Il ne s'agit pas d'un traitement validé, mais d'une piste de recherche active. En parler à votre professionnel de santé reste la meilleure démarche.
Suivre vos symptômes au quotidien permet de repérer vos propres seuils, d'anticiper les périodes difficiles et de mieux communiquer avec votre équipe soignante.
Essayer Boussole gratuitementSources
- Watai K, Taniguchi M, Azuma K. The Gut-Brain-Immune Axis in Environmental Sensitivity Illnesses. Int J Mol Sci. 2025;26(20):9997. DOI — PMID 41155291
- Guo C, et al. Deficient butyrate-producing capacity in the gut microbiome is associated with bacterial network disturbances and fatigue symptoms in ME/CFS. Cell Host Microbe. 2023;31(2):288-304. DOI — PMID 36758522
- Nikolova R, et al. Gut Microbiome and Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS): Insights into Disease Mechanisms. Int J Mol Sci. 2025;27(1):425. DOI — PMID 41516296
- Lanzara R, et al. Gut Microbiota and Psychological Distress in Fibromyalgia: A Systematic Review. Biopsychosoc Sci Med. 2026. DOI — PMID 41504323
- Siracusa R, et al. Fibromyalgia: Pathogenesis, Mechanisms, Diagnosis and Treatment Options Update. Int J Mol Sci. 2021;22(8):3891. DOI
- Shtrozberg S, et al. Is the gut microbiome of importance in fibromyalgia? A critical review of emerging evidence. Clin Exp Rheumatol. 2025;43(6):990-998. DOI — PMID 40576702
- Caliman-Sturdza OA, et al. Microbiome and Long COVID-19: Current Evidence and Insights. Int J Mol Sci. 2025;26(20):10120. DOI — PMID 41155411
- Liew F, et al. Large-scale phenotyping of patients with long COVID post-hospitalization reveals mechanistic subtypes of disease. Nat Immunol. 2024;25(4):607-621. DOI — PMID 38589621