Pourquoi le Covid long s'emballe : piliers mécanistiques et facteurs amplificateurs
Persistance virale, neuroinflammation, dysautonomie, dérégulation immunitaire : les piliers mécanistiques du Covid long s'alimentent mutuellement autour d'un hub central, le système nerveux autonome. Identifier les facteurs amplificateurs est la clé pour prioriser les interventions.
Vous cherchez à comprendre pourquoi votre Covid long ne disparaît pas et pourquoi les symptômes s'aggravent parfois sans raison apparente.
Hub central
Le système nerveux autonome coordonne tous les piliers. Quand il se dérègle, tout le système suit.
6 piliers interdépendants
Inflammation, vaisseaux, énergie, intestin, nerfs, histamine cérébrale : aucun n'agit seul, tous s'entretiennent.
Histamine cérébrale
Le TMN régule l'éveil et la cognition via H1/H3R. Silencié par la neuroinflammation Covid, il contribue au brouillard mental persistant.
Amplificateurs documentés
Surmenage, sommeil, stress biologique et désordre digestif abaissent les seuils de tolérance.
Cercle vicieux
Chaque pilier aggrave les autres. La sortie passe par la réduction de la charge globale.
📖 Termes de référence
- Système nerveux autonome (SNA) = Autonomic Nervous System (ANS)
- Dysautonomie = Dysautonomia
- Malaise post-effort (PEM) = Post-Exertional Malaise (PEM)
- Variabilité de la fréquence cardiaque (VFC) = Heart Rate Variability (HRV)
- Neuropathie des petites fibres (NPF) = Small Fiber Neuropathy (SFN)
- Noyau tubéro-mamillaire (TMN) = Tuberomammillary Nucleus
- Histamine N-méthyltransférase (HMT) = Histamine N-methyltransferase — enzyme de dégradation intraneuronale
- Récepteur H3 (H3R) = Histamine H3 receptor (autorécepteur présynaptique)
- Syndrome de tachycardie posturale orthostatique = Postural Orthostatic Tachycardia Syndrome (POTS)
- Barrière hémato-encéphalique (BHE) = Blood-Brain Barrier (BBB)
- Phosphorylation oxydative = Oxidative Phosphorylation (OXPHOS)
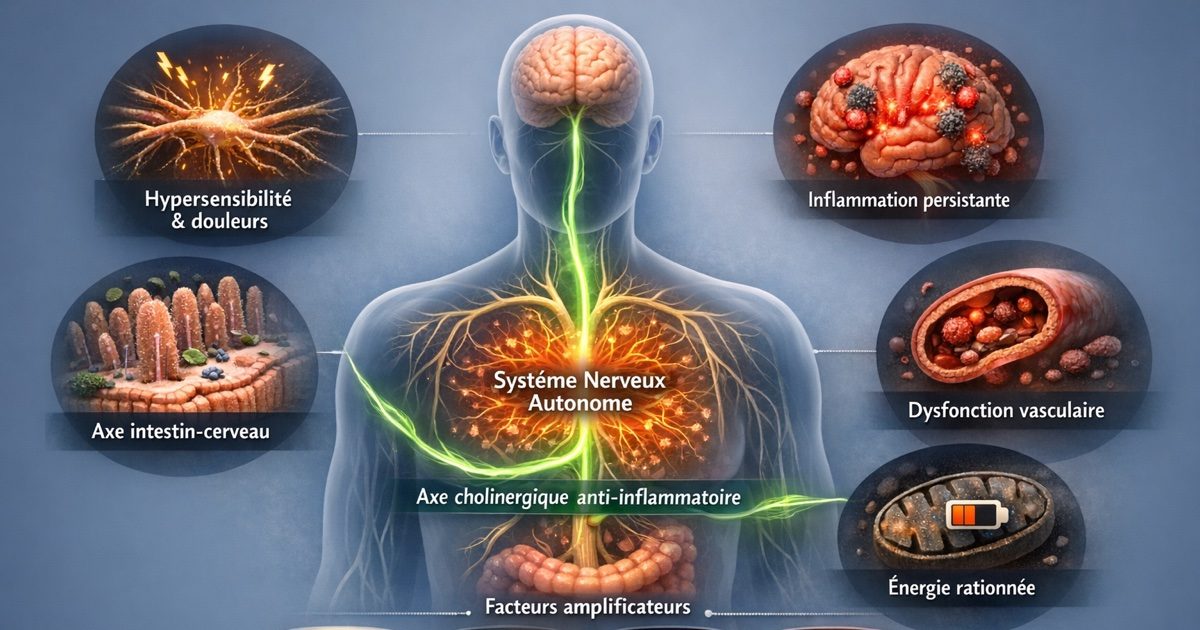
Une maladie de la régulation, pas de la destruction
🟠 Association documentée — consensus ME/CFS et Covid longQuand une personne consulte pour un Covid long, les examens reviennent souvent dans les normes. La NFS est correcte, la CRP est basse, l'imagerie ne montre rien. Pourtant, la fatigue est invalidante, le brouillard mental persiste, l'effort déclenche des crashs disproportionnés.
Cette situation n'est pas un mystère — elle est un indice. Le Covid long ne détruit pas les organes comme le ferait un infarctus ou une cirrhose. Il dérègle la manière dont ces organes se coordonnent[1]. Les outils médicaux classiques, conçus pour détecter des lésions stables et des anomalies nettes, peinent à capturer ces dysfonctionnements fonctionnels, fluctuants et dépendants du contexte.
Le système nerveux autonome, la microcirculation, l'immunité et le métabolisme énergétique peuvent apparaître normaux au repos et devenir inadaptés à l'effort, au stress ou à la charge cognitive. C'est cette variabilité qui fait du Covid long une maladie déroutante — et qui explique pourquoi l'approche mono-organe échoue systématiquement.
Ces 6 piliers s'alimentent mutuellement autour d'un hub central — le système nerveux autonome. Une hypothèse de plus en plus documentée suggère qu'un réservoir viral persistant pourrait constituer leur déclencheur commun : des fragments du SARS-CoV-2 résiduels dans les tissus entretiendraient la stimulation immunitaire qui alimente l'ensemble de la cascade.
Le Covid long appartient aux maladies de la régulation : les organes fonctionnent, mais leur coordination est perturbée.
Le hub central : le système nerveux autonome sous pression
🟠 Association documentée — Nature Reviews Cardiology 2024Le système nerveux autonome est le pilotage automatique de l'organisme. Il ajuste en permanence la fréquence cardiaque, la tension artérielle, la digestion, la thermorégulation et la réponse à l'effort — le tout sans contrôle conscient. Son équilibre repose sur deux branches complémentaires : le sympathique (alerte, action, mobilisation d'énergie) et le parasympathique (récupération, digestion, réparation), véhiculé principalement par le nerf vague.
Dans le Covid long, ce pilotage se dérègle. La dysautonomie cardiovasculaire post-COVID pourrait concerner environ un tiers des personnes hautement symptomatiques, selon une revue publiée dans Nature Reviews Cardiology[2]. Elle se manifeste par un syndrome de tachycardie posturale orthostatique (POTS), une tachycardie sinusale inappropriée, une hypotension orthostatique ou des syncopes réflexes.
Mais le SNA ne régule pas que le cœur. Il contrôle aussi l'inflammation — et c'est un point fondamental pour comprendre pourquoi il occupe la position de hub central dans cette cascade.
L'axe cholinergique anti-inflammatoire : le frein qui lâche
À l'interface entre le cerveau et le système immunitaire se trouve un mécanisme discret mais essentiel : l'axe cholinergique anti-inflammatoire. Lors d'une réponse immunitaire normale, le nerf vague libère de l'acétylcholine qui agit sur des récepteurs présents à la surface de cellules immunitaires, réduisant la production de cytokines pro-inflammatoires. Ce n'est pas de l'immunosuppression — c'est un frein permettant à l'inflammation de décroître une fois la menace contrôlée.
Quand ce frein dysfonctionne, l'inflammation ne s'éteint pas complètement. Il en résulte une inflammation de bas grade, fluctuante, coûteuse en énergie et qui interagit avec tous les autres piliers[3]. C'est pourquoi une dysautonomie isolée n'existe quasiment jamais dans le Covid long : quand le SNA se dérègle, l'immunité, la circulation et l'énergie suivent.
Le SNA ne régule pas seulement le cœur — il contrôle aussi l'inflammation via l'axe cholinergique. Quand ce hub se dérègle, les 6 piliers s'activent en cascade.
Pilier 1 — L'inflammation qui ne s'éteint pas
🟠 Association documentée — cohortes observationnelles et études mécanistiquesL'immunité ne s'éteint pas complètement après l'infection. Elle reste en alerte de bas grade, ce qui consomme beaucoup d'énergie et entretient la fatigue — même quand les analyses sanguines sont normales. La neuroinflammation qui en résulte contribue directement au brouillard mental.
Voir le détail ↓Parler de dérégulation immunitaire dans le Covid long ne signifie pas que le système immunitaire est en permanence suractivé. La CRP peut être normale. Les bilans inflammatoires standards peuvent être rassurants. Le problème est plus subtil : l'immunité ne parvient plus à se résoudre correctement après l'alerte initiale[4].
Cette transition incomplète se traduit par une activation prolongée de certaines composantes de l'immunité innée (monocytes, macrophages, mastocytes), une réponse adaptative parfois épuisée, et des signaux de freinage altérés. L'activation endothéliale qui en résulte mobilise la voie NF-κB/NLRP3, avec formation de pièges extracellulaires à neutrophiles (NETose) et une tempête cytokinique de bas grade[5].
La neuroinflammation persistante, avec activation microgliale et rupture partielle de la barrière hémato-encéphalique, constitue un relais direct vers les symptômes cognitifs[6]. Cette immunité résiduelle est coûteuse : maintenir même partiellement le système immunitaire en alerte consomme une quantité importante d'énergie et de ressources métaboliques, contribuant directement à la fatigue chronique.
Cette dissociation entre fatigue subjective et biomarqueurs circulants est désormais documentée de façon rigoureuse. Une étude contrôlée (Omdal et al., Brain Behav Immun Health, 2026, n = 96) a mesuré chez 48 personnes avec Covid long (critères NICE) appariées à 48 témoins guéris une fatigue invalidante — fVAS médian 63 vs 5 (p < 0,001), FACIT-F 21,5 vs 49 (p < 0,001) — sans qu'aucun des biomarqueurs périphériques ne diffère entre groupes : CRP, TNF-α, IL-6, HSP90α, Serpin F1, hémopexine, APOA4 tous normaux. Les ANA positifs (10,4 %) ne corrèlent pas avec la sévérité. En analyse multivariée, aucune association biomarqueur-fatigue n'est significative. Ce résultat déplace la question mécanistique : la fatigue du Covid long n'est pas soutenue par l'inflammation systémique classique mesurable en périphérie — les candidats les plus plausibles restent la neuroinflammation confinée au SNC, les modifications épigénétiques, ou une dérégulation du traitement prédictif cérébral non reflétés dans le sang[28].
La stimulation magnétique transcrânienne répétitive (rTMS) est une piste non invasive étudiée pour moduler ces circuits dysfonctionnels — ce que dit la science.
Mais pourquoi l'immunité innée reste-t-elle en alerte des mois après l'infection ? Une hypothèse aujourd'hui bien documentée est celle de la persistance virale : des fragments du SARS-CoV-2 — protéine spike, ARN, nucléocapside — peuvent persister dans certains tissus et stimuler en continu les récepteurs de l'immunité innée, alimentant ce bas grade inflammatoire. Des données suggèrent que la protéine spike circule dans le plasma jusqu'à 12 mois après l'infection chez des personnes avec Covid long, alors qu'elle est absente chez celles ayant récupéré sans séquelles. Ces résidus, même non réplicatifs, pourraient constituer le signal d'alarme permanent qui empêche la résolution immunitaire. → Lire l'article complet sur la persistance virale et les réservoirs tissulaires
Pilier 2 — Quand le sang circule mal
🟠 Association documentée — dysfonction endothéliale et coagulationLe sang circule mal dans les plus petits vaisseaux. L'oxygène et les nutriments arrivent insuffisamment aux muscles et au cerveau au moment de l'effort — d'où la fatigue rapide, la récupération lente et le brouillard cognitif, même avec une saturation en oxygène normale au doigt.
Voir le détail ↓L'énergie peut être produite, mais mal distribuée. La microcirculation — le réseau des plus petits vaisseaux, tapissé par l'endothélium — assure l'acheminement de l'oxygène et des nutriments au plus près des cellules. Dans le Covid long, l'endothélium ne fonctionne plus comme un régulateur fin mais comme une surface dysfonctionnelle[5].
L'hypoperfusion qui en résulte est fonctionnelle : la saturation en oxygène mesurée au doigt peut être normale, mais la distribution fine au niveau des tissus est inadaptée au moment de la demande. Les muscles fatiguent rapidement malgré un effort modéré, la récupération est lente, et le cerveau — extrêmement sensible aux variations de perfusion — produit un brouillard cognitif[6].
Les anomalies de la coagulation de bas grade (activation plaquettaire, fibrine anormale, micro-agrégats) aggravent cette dysfonction. Il ne s'agit pas d'une maladie thrombotique classique avec des caillots visibles à l'imagerie, mais d'un état immuno-thrombotique dynamique, dépendant du contexte inflammatoire et neuro-végétatif. Certaines personnes décrivent des mains froides, des doigts qui changent de couleur, une thermosensibilité anormale — autant de signes évocateurs d'une dysfonction microvasculaire périphérique.
Pilier 3 — L'énergie rationnée
🟠 Association documentée — dysfonction mitochondriale post-COVIDLes mitochondries (centrales énergétiques des cellules) fonctionnent en mode dégradé. Elles produisent moins d'énergie et tolèrent mal les augmentations de demande — c'est ce qui provoque les crashs après un effort même modéré (malaise post-effort).
Voir le détail ↓Les mitochondries sont les centrales énergétiques de chaque cellule. Dans le Covid long, elles ne sont pas détruites — elles fonctionnent en mode dégradé. Exposées à un environnement inflammatoire persistant, à une hypoperfusion intermittente et à des signaux de stress neuro-végétatif, elles adoptent un régime protecteur : diminution de la production d'ATP, limitation de la capacité d'adaptation à l'effort, augmentation du stress oxydatif[9].
Des travaux récents montrent que cette suppression énergétique peut persister au moins 60 jours après l'infection, avec une réduction durable de la β-oxydation des acides gras et de la phosphorylation oxydative dans le muscle squelettique — sans invasion virale directe. Le mécanisme passe par l'action combinée de l'interféron-γ et du TNF-α sur les myotubes[10].
Certains modèles intégratifs considèrent la dysfonction mitochondriale comme un amplificateur secondaire plutôt qu'un pilier autonome. En pratique, la distinction dépend du stade : initiée par l'inflammation et l'hypoperfusion, elle devient un facteur limitant indépendant une fois installée. La protéine WASF3, liée au stress du réticulum endoplasmique, pourrait jouer un rôle dans cette bascule vers une dysfonction auto-entretenue[11].
Ce pilier explique un phénomène central : le malaise post-effort. Toute augmentation brutale de la demande énergétique dépasse la capacité mitochondriale, entraînant une aggravation retardée des symptômes. Ce n'est ni du déconditionnement ni de la fragilité psychologique — c'est une limitation physiologique mesurable[12].
Les mitochondries ne sont pas détruites — elles fonctionnent en régime de protection, avec des conséquences directes sur la tolérance à l'effort.
Pilier 4 — L'axe intestin-cerveau : le signal toxique
🟠 Association documentée — cohortes endoscopiques et microbioteL'intestin communique en permanence avec le cerveau via le nerf vague. Quand la barrière intestinale devient plus perméable et que le microbiote est déséquilibré, des signaux inflammatoires remontent au cerveau et perturbent l'humeur, le sommeil et la cognition.
Voir le détail ↓L'intestin abrite une grande partie du système immunitaire et communique en permanence avec le cerveau via le nerf vague. Quand la barrière intestinale devient plus perméable — même modérément — des molécules normalement confinées franchissent la muqueuse et activent le système immunitaire systémique. Cette stimulation n'est ni massive ni constante, mais suffisante pour entretenir la dérégulation[13].
Un facteur sous-estimé dans cette dysfonction muqueuse est la persistance virale intestinale. Des études endoscopiques prospectives montrent que la protéine nucléocapside du SARS-CoV-2 est détectable dans la muqueuse gastro-intestinale haute chez environ 37% des personnes ayant un antécédent de Covid-19 — indépendamment du statut vaccinal ou du nombre d'infections antérieures. Cette persistance locale pourrait entretenir directement l'inflammation muqueuse et la perméabilité accrue, créant les conditions d'une dysbiose auto-entretenue. → Données détaillées sur le réservoir gastro-intestinal
Le microbiote intestinal joue un rôle central dans ce processus. Un déséquilibre (dysbiose) peut amplifier l'inflammation, perturber la tolérance immunitaire et modifier le métabolisme du tryptophane — précurseur de la sérotonine. Quand cette voie est déviée vers la production de kynurénine au lieu de sérotonine (mécanisme NF-κB/IL-6/IDO1 détaillé ici), les conséquences touchent à la fois l'humeur, le sommeil et la cognition[14].
Des interventions ciblant le microbiote (probiotiques, prébiotiques, transplantation fécale) ont montré des améliorations sur la fatigue, la cognition et le sommeil dans des études préliminaires[15]. Ces résultats ne sont ni universels ni immédiats, mais ils s'inscrivent dans une logique cohérente : quand l'axe intestin-immunité-cerveau s'améliore, il peut faciliter la restauration progressive des autres systèmes.
Pilier 5 — Les nerfs à vif
🟠 Association documentée — neuropathie petites fibres, cohortes biopsieLes petites fibres nerveuses qui régulent la sensation cutanée et le tonus vasculaire sont endommagées chez une majorité de personnes atteintes de Covid long. Cela explique les douleurs de type brûlure, l'hypersensibilité au bruit et à la lumière, et la sensation permanente de malaise grippal.
Voir le détail ↓Les douleurs du Covid long ne sont pas imaginaires, et elles ne relèvent pas toujours d'une inflammation classique. Une cohorte de 18 personnes souffrant de douleurs neuropathiques post-COVID a révélé des biopsies cutanées anormales chez 82 % d'entre elles, avec une densité réduite de fibres nerveuses épidermiques — le signe d'une neuropathie des petites fibres[16].
Cette neuropathie des petites fibres post-COVID se manifeste par des douleurs de type brûlure, des paresthésies, des sensations de formication, et une hypersensibilité sensorielle. Elle coexiste fréquemment avec la dysautonomie — logique, puisque les petites fibres nerveuses régulent à la fois la sensation cutanée et le tonus vasculaire périphérique[17].
Ce pilier permet de comprendre pourquoi certaines personnes décrivent une sensation permanente de malaise grippal, une intolérance au bruit et à la lumière, ou des douleurs migrantes sans cause apparente. Ce ne sont pas des symptômes isolés — ce sont les manifestations d'un système nerveux périphérique en souffrance.
Pilier 6 — Histamine, mastocytes, orexine : le triangle qui dérègle le sommeil et l'éveil
🟠 Mécanisme proposé — données convergentes MCAS et Covid longDans le cerveau, l'histamine n'est pas qu'une molécule d'allergie : elle régule l'éveil, la cognition et le sommeil. Quand les mastocytes sont suractivés et que le système orexine est perturbé, le résultat est un cycle veille-sommeil déréglé avec des réveils nocturnes, une somnolence diurne et un brouillard mental.
Voir le détail ↓L'histamine est surtout connue pour son rôle dans les allergies. Dans le cerveau, elle est un neuromédiateur à part entière, produit par une seule structure : le noyau tubéro-mamillaire (TMN), situé dans l'hypothalamus postérieur. Ses projections atteignent le cortex, l'hippocampe et le thalamus. Via les récepteurs H1 (excitateurs), elle maintient l'éveil et soutient la vigilance. Via le récepteur H3 (autorécepteur présynaptique), elle régule sa propre libération par rétrocontrôle négatif — et module finement la cognition, la mémoire de travail et la vitesse de traitement cérébral[19].
Une seconde source d'histamine cérébrale existe : les mastocytes des méninges. Positionnés au contact des fibres du nerf trijumeau et des vaisseaux méningés, ils libèrent de l'histamine lors d'une stimulation immune ou inflammatoire. Cette histamine méningée active la microglie, entretient une neuroinflammation localisée et perturbe le fonctionnement de l'hypothalamus — y compris le TMN lui-même. Dans le Covid long, des données suggèrent que des mastocytes stimulés par des signaux pathogènes activent la microglie hypothalamique, créant les conditions d'un brouillard mental d'origine neuroimmune[20]. Des données in vivo montrent qu'un antagoniste du récepteur H3 restaure la neurogenèse hippocampique et les fonctions cognitives dans un modèle de neuroinflammation induite par LPS, via la voie PKA/CREB et la suppression de NF-κB[21].
Dans le contexte du Covid long, ces deux systèmes histaminergiques semblent perturbés simultanément. Le SARS-CoV-2 active les mastocytes par des voies IgE-like et MRGPRX2, amplifiant la libération d'histamine méningée. En parallèle, la neuroinflammation chronique dérègle la signalisation H3R dans les circuits de l'éveil, de la mémoire et de l'attention. Des cas de rémission complète d'un POTS hyperadrénergique post-Covid sous bloqueurs histaminiques H1 et H2 ont été documentés, suggérant que la cascade histamine-dysautonomie est fonctionnellement réversible[22].
Le système orexinergique complète ce tableau. Les neurones à orexine, situés dans l'hypothalamus latéral, excitent directement les neurones histaminergiques du TMN via les récepteurs OX2R — c'est ce signal qui maintient l'éveil stable[25][26]. La relation est réciproque : les axones histaminergiques innervent aussi les neurones orexine, mais le sens dominant pour l'éveil est orexine → histamine. Lorsque la neuroinflammation, l'activation mastocytaire ou la dérégulation hypothalamique perturbent le système orexinergique, les neurones histaminergiques du TMN perdent leur excitation tonique. Le résultat : une instabilité du cycle veille-sommeil — somnolence diurne excessive, sommeil fragmenté, réveils nocturnes et architecture du sommeil désorganisée. Chez la souris, la perte du récepteur OX2R suffit à elle seule à abolir l'excitation des neurones histaminergiques et à déclencher des attaques de sommeil NREM[27].
Ce mécanisme orexine-histamine-sommeil crée un cercle vicieux propre au Covid long : la neuroinflammation perturbe les neurones orexine → les neurones histaminergiques du TMN perdent leur excitation → le sommeil devient non réparateur → le sommeil non réparateur aggrave la neuroinflammation → la boucle se referme.
Le cercle vicieux orexine → histamine → sommeil dans le Covid long. Chaque étape aggrave la suivante — le sommeil non réparateur relance la neuroinflammation qui a initié la cascade.
L'histamine cérébrale n'est pas un pilier isolé : elle amplifie la dysautonomie (pilier SNA), perd son excitation tonique lorsque l'orexine dysfonctionne — perturbant le sommeil réparateur — et contribue directement au brouillard mental, signal transversal décrit en section suivante.
Le TMN produit l'histamine neuronale nécessaire à l'éveil et à la cognition. Les mastocytes méningés constituent une seconde source, pro-inflammatoire, pouvant perturber ce même système via la microglie hypothalamique.
👁️ L'œil du Docteur en pharmacie — SAMe, HNMT et sous-méthylation
La HNMT appartient à la famille des méthyltransférases SAM-dépendantes[23] : elle utilise le SAMe (S-adénosylméthionine) comme unique donneur de méthyle pour convertir l'histamine en télé-méthylhistamine inactive. C'est la seule voie d'inactivation de l'histamine dans le SNC — contrairement à la DAO (diamine oxydase) qui domine en périphérie[24].
La conséquence directe : si le SAMe est insuffisant, la HNMT manque de substrat méthyl-donneur, et l'histamine synaptique s'accumule. Des souris dont le gène HNMT est invalidé présentent une élévation dramatique de l'histamine cérébrale, avec fragmentation du cycle veille-sommeil par excès d'activation H1R — exactement le tableau clinique du Covid long[24].
Or, un déficit fonctionnel en SAMe est un mécanisme transversal documenté dans le Covid long et les états d'inflammation chronique : la demande en groupements méthyle augmente massivement (méthylation de l'ARN viral, synthèse de créatine, neurotransmission), épuisant le pool disponible. C'est précisément ce que couvre l'article Méthylation et cerveau : quand un déficit invisible dérègle tout →
Hypothèse mécanistique non encore testée directement dans le Covid long par mesure conjointe SAMe/t-méthylhistamine — mais cohérente avec l'ensemble des données disponibles sur HNMT et méthylation. À retenir comme piste d'exploration clinique, pas comme conclusion établie.
Les amplificateurs : ce qui fait basculer
🟠 Mécanismes proposés — cohérence avec données PEM, dysautonomie, microbioteLes 6 piliers décrivent les mécanismes. Mais la cascade ne tourne pas en vase clos. Elle est modulée en permanence par des facteurs capables d'abaisser les seuils de tolérance et de provoquer des rechutes.
Le malaise post-effort (PEM)
Quand la demande énergétique dépasse la capacité mitochondriale, l'organisme paie l'activité comme une dette — avec un délai de 24 à 72 heures. Ce n'est pas un manque de volonté, c'est un dépassement physiologique mesurable. Forcer dans ce contexte verrouille le syndrome au lieu de le résoudre. Comprendre le pacing →
Le sommeil perturbé
Le sommeil est le principal mécanisme de restauration de la régulation. Quand il est altéré — endormissement difficile, sommeil non réparateur, réveils précoces — la résolution immunitaire est empêchée, la fatigue centrale s'aggrave et les seuils de tolérance s'effondrent. Un tonus vagal insuffisant peut expliquer l'échec de la transition vers le sommeil profond[18].
Le stress comme charge biologique
Le stress ne désigne pas ici un état psychologique subjectif, mais une charge biologique globale mobilisant les systèmes nerveux, endocriniens et immunitaires. L'infection elle-même est un stress majeur. L'incertitude, la perte de repères et l'errance diagnostique ajoutent une charge supplémentaire qui abaisse les seuils et perturbe la récupération.
Le désordre digestif
La dysbiose intestinale entretient l'inflammation systémique qui alimente la fatigue qui aggrave la dysbiose — un cercle vicieux spécifique au pilier 4.
L'activation mastocytaire périphérique
Chez certaines personnes, les mastocytes périphériques — présents dans la peau, les poumons et la muqueuse digestive — restent en état d'alerte chronique : intolérances alimentaires, flushs, palpitations, hypersensibilité sensorielle. Cette activation amplifie la perméabilité vasculaire (pilier 2), la transmission nerveuse périphérique (pilier 5) et l'inflammation muqueuse intestinale (pilier 4). Pour le volet cérébral de l'histamine — TMN et mastocytes méningés — voir le Pilier 6.
La surcharge thérapeutique
Un amplificateur souvent négligé : la multiplication d'examens, de compléments non hiérarchisés et de protocoles contradictoires. Chaque intervention mobilise des ressources et crée des attentes. Dans un système déjà fragilisé, l'excès de soins peut entretenir la cascade qu'il cherche à corriger.
Tant que les seuils sont respectés, l'organisme compense. Les amplificateurs abaissent la marge adaptative jusqu'à la bascule.
Le cercle vicieux — et le brouillard mental comme signal transversal
🔴 Modèle intégratif — consensus clinique, données mécanistiques partiellesAucun de ces piliers ne fonctionne de manière isolée. L'inflammation entretient la dysfonction endothéliale. L'hypoperfusion aggrave la fatigue mitochondriale. La dysbiose intestinale alimente l'inflammation. La dysautonomie perturbe tout le reste. Et chaque amplificateur accélère la boucle.
Au centre de ce cercle se trouve le brouillard mental — non pas comme un pilier supplémentaire, mais comme le signal transversal que l'ensemble du système est sous contrainte. Le cerveau, soumis à un environnement biologique instable, adopte un fonctionnement protecteur : il réduit les fonctions les plus coûteuses (vitesse de traitement, multitâche, endurance attentionnelle) pour préserver son intégrité. Ce ralentissement n'est pas psychologique — c'est une stratégie de survie énergétique.
La fatigue centrale du Covid long ne correspond pas à une perte de motivation. Le désir d'agir peut être intact. C'est la capacité neuro-énergétique qui fait défaut. La récupération cérébrale dépend directement de l'amélioration des contraintes périphériques : tant que l'immunité reste mal résolue, que la microcirculation est instable ou que la régulation autonome est défaillante, le cerveau maintient son mode de protection.
Cette lecture permet de sortir d'une alternative stérile : soit tout est psychologique, soit tout est neurologique. Le Covid long se situe dans un espace intermédiaire où la clinique précède encore largement la compréhension mécanistique complète — et où comprendre est la condition nécessaire pour cesser d'aggraver.
La boucle auto-entretenue : les 6 piliers s'alimentent mutuellement. Le brouillard mental est le signal central de surcharge systémique.
👁️ L'œil du Docteur en pharmacie
Certaines molécules agissent simultanément sur plusieurs piliers de cette cascade. Le coenzyme Q10 (ubiquinol) soutient la chaîne respiratoire mitochondriale et possède des propriétés antioxydantes documentées dans le ME/CFS. Le magnésium intervient dans la production d'ATP, la régulation neuro-musculaire et le tonus vagal. Les oméga-3 (EPA/DHA) modulent l'inflammation via les résolvines et protectines. Des probiotiques ciblés pourraient améliorer la perméabilité intestinale et réduire les signaux inflammatoires systémiques.
La taurine, dont un déficit plasmatique a été documenté dans le Covid long, montre des effets anti-inflammatoires et métaboliques qui mériteraient d'être évalués plus largement. Les mécanismes et les données cliniques disponibles sont détaillés dans : Taurine et Covid long : pourquoi votre corps en manque et ce que dit la recherche. L'ivermectine s'inscrit dans le même espace d'exploration, avec des effets potentiels sur plusieurs de ces piliers — voir notre analyse des mécanismes et essais disponibles. Ces molécules font partie des candidats les plus actifs dans les 6 RCT Covid long 2024-2025 actuellement en recrutement ou en analyse.
Un point essentiel : la multiplication de compléments sans hiérarchie ni suivi constitue en soi un facteur d'instabilité. Chaque substance mobilise des voies métaboliques, crée des interactions potentielles et peut devenir contre-productive si elle est mal dosée ou mal séquencée. En parler à votre professionnel de santé reste indispensable — et séquencer les interventions plutôt que les empiler est souvent plus efficace.
🧩 Ce que l'on sait — et ce que l'on ne sait pas encore
Ce que les données soutiennent : La dysautonomie post-COVID est documentée dans plusieurs cohortes et revues systématiques. La dysfonction endothéliale et l'hypoperfusion tissulaire sont objectivées par des mesures fonctionnelles. La dysfonction mitochondriale persiste au-delà de la phase aiguë, avec des mécanismes identifiés (IFN-γ, TNF-α, WASF3). La neuropathie des petites fibres est confirmée par biopsie cutanée dans des cohortes post-COVID.
Ce qui reste spéculatif ou incomplet : La hiérarchie exacte entre piliers varie d'une personne à l'autre — il n'existe pas encore de biomarqueur universel pour prédire quel pilier domine. Le rôle précis de l'axe cholinergique anti-inflammatoire chez l'humain est plausible mais non mesurable directement en pratique clinique. L'efficacité des interventions ciblant le microbiote est prometteuse mais repose sur des études de petite taille.
Cet article présente des mécanismes et des pistes de recherche. Les molécules citées (CoQ10, magnésium, oméga-3, taurine, ivermectine) ne constituent pas des recommandations thérapeutiques.
① Ivermectine : usage hors-AMM strict en France pour le Covid long — aucune étude contrôlée concluante à ce jour, risque de toxicité neurologique à doses élevées. Ne pas s'auto-prescrire.
② CoQ10 + statines : si vous prenez des statines, une supplémentation en CoQ10 doit être discutée avec votre médecin (interaction pharmacologique directe sur la synthèse du mévalonate).
③ Oméga-3 à doses élevées : effet antiagrégant plaquettaire — à signaler si traitement anticoagulant ou antiagrégant en cours (risque hémorragique potentialisé).
En cas de doute sur l'adéquation de ces approches à votre situation, parlez-en à votre médecin ou pharmacien.
Ce qu'il faut retenir
Le Covid long n'est pas une seule maladie mais un réseau de six mécanismes biologiques qui s'entretiennent mutuellement — inflammasome, vasculopathie, dysfonction mitochondriale, dysbiose, neuropathie des petites fibres, dérégulation histamine/mastocytes — avec le système nerveux autonome comme pivot central. Cette imbrication explique pourquoi les bilans standards reviennent normaux et pourquoi les bonnes journées alternent avec les mauvaises sans logique apparente.
Comprendre cette carte ne donne pas de solution immédiate, mais elle change radicalement la façon de prioriser les explorations et de parler à ses soignants. Chercher LA cause est une impasse ; identifier les leviers accessibles est une stratégie.
Questions fréquentes
🟢 Réponses issues du corpus scientifique — niveau intermédiairePourquoi le Covid long touche autant de systèmes différents ?
Parce que le système nerveux autonome régule simultanément la fréquence cardiaque, la tension, la digestion, l'inflammation et l'énergie. Quand ce pilotage se dérègle, tous les systèmes qu'il coordonne dysfonctionnent en cascade.
Peut-on avoir un Covid long avec des examens normaux ?
Oui. Les examens standards détectent des lésions structurelles, pas des dérèglements fonctionnels. Le Covid long est souvent un trouble de la régulation : les organes sont intacts, mais leur coordination est altérée.
Le stress aggrave-t-il le Covid long ?
Le stress — au sens biologique, pas uniquement psychologique — constitue un amplificateur documenté. Il abaisse les seuils de tolérance, perturbe le sommeil et renforce la dysautonomie.
Pourquoi l'effort aggrave les symptômes ?
Quand la capacité mitochondriale est réduite, toute demande énergétique qui dépasse le seuil déclenche un malaise post-effort retardé. C'est une limitation physiologique, pas un manque de volonté.
Suivre vos symptômes au quotidien permet de repérer vos propres seuils et d'adapter votre charge.
Essayer l'app gratuitementSources
🟢 24 sources — revues à comité de lecture- Steiner S, et al. Understanding, diagnosing, and treating ME/CFS — State of the art: Report of the 2nd international meeting at the Charité Fatigue Center. Autoimmun Rev. 2023;22(11):103452. DOI
- Fedorowski A, et al. Cardiovascular autonomic dysfunction in post-COVID-19 syndrome: a major health-care burden. Nat Rev Cardiol. 2024;21(6):379-395. DOI
- Jammoul M, et al. Investigating the possible mechanisms of autonomic dysfunction post-COVID-19. Auton Neurosci. 2022;245:103071. DOI
- Talkington GM, et al. Neurological sequelae of long COVID: a comprehensive review. Front Neurol. 2025;15:1465787. DOI
- Valencia I, et al. Mechanisms of endothelial activation, hypercoagulation and thrombosis in COVID-19. Cardiovasc Diabetol. 2024;23(1):75. DOI
- Shabani Z, et al. Vascular dysfunctions contribute to the long-term cognitive deficits following COVID-19. Biology. 2023;12(8):1106. DOI
- Tang SW, et al. Long COVID, neuropsychiatric disorders, psychotropics, present and future. Acta Neuropsychiatr. 2022;34(3):109-126. DOI
- Qu C, et al. Could histamine H1 receptor antagonists be used for treating COVID-19? Int J Mol Sci. 2021;22(11):5672. DOI
- Molnar T, et al. Mitochondrial dysfunction in long COVID: mechanisms, consequences, and potential therapeutic approaches. GeroScience. 2024;46(5):5267-5286. DOI
- Homma ST, et al. Respiratory SARS-CoV-2 infection causes skeletal muscle atrophy and long-lasting energy metabolism suppression. Biomedicines. 2024;12(7):1443. DOI
- Syed AM, et al. Mitochondrial dysfunction in ME/CFS. Physiology. 2025;40(4). DOI
- Mantle D, et al. Mitochondrial dysfunction and CoQ10 supplementation in post-viral fatigue syndrome. Int J Mol Sci. 2024;25(1):574. DOI
- Kim DY, et al. Brain-gut axis-based treatments in Long COVID and ME/CFS. J Transl Med. 2026;24(1). DOI
- King LR. Gastrointestinal manifestations of long COVID. Life Sci. 2024;357:123100. DOI
- Lau RI, et al. Long COVID and gut microbiome: insights into pathogenesis and therapeutics. Gut Microbes. 2025;17(1):2457495. DOI
- Drobinska N, et al. Small fiber neuropathy in long COVID: a cohort study. Eur Neurol. 2025;88(2):52-63. DOI
- Oaklander AL. Increasing associations of long-COVID with small-fiber neuropathy. Pain. 2024;165(9):e93-e95. DOI
- Polizzi J, et al. Resonant breathing improves self-reported symptoms and wellbeing in people with Long COVID. Front Rehabil Sci. 2024;5:1411344. DOI
- Thakkar MM. Histamine in the regulation of wakefulness. Sleep Med Rev. 2011;15(1):65-74. DOI
- Hassan L, et al. An unusual case of blackout in a COVID-19 patient: COVID-19 brain fog. Cureus. 2023;15(3):e36273. DOI
- Wang J, et al. Histamine H3R antagonist counteracts the impaired hippocampal neurogenesis in lipopolysaccharide-induced neuroinflammation. Int Immunopharmacol. 2022;110:109045. DOI
- González-Alvarez F, et al. Complete remission with histamine blocker in a patient with intractable hyperadrenergic POTS secondary to long-COVID. J Hypertens. 2024;42(5):928-932. DOI
- Li J, et al. Insights into S-adenosyl-l-methionine (SAM)-dependent methyltransferase related diseases and genetic polymorphisms. Mutat Res Rev Mutat Res. 2022;788:108396. DOI
- Yoshikawa T, et al. Analysis of brain histamine clearance using genetically engineered mice. Nihon Yakurigaku Zasshi. 2018;152(1):16-20. DOI
- Eriksson KS, Sergeeva O, Brown RE, Haas HL. Orexin/hypocretin excites the histaminergic neurons of the tuberomammillary nucleus. J Neurosci. 2001;21(23):9273-9279. DOI
- Bayer L, Eggermann E, Serafin M, et al. Orexins (hypocretins) directly excite tuberomammillary neurons. Eur J Neurosci. 2001;14(9):1571-1575. DOI
- Willie JT, Chemelli RM, Sinton CM, Yanagisawa M, et al. Distinct narcolepsy syndromes in Orexin receptor-2 and Orexin null mice. Neuron. 2003;38(5):715-730. DOI
- Omdal R, et al. Persistent fatigue in long-COVID is not associated with peripheral inflammatory or cellular stress biomarkers: A cross-sectional controlled study. Brain Behav Immun Health. 2026;54:101226. DOI · PMID 42004496. n=96, 48 Covid long vs 48 témoins guéris — fatigue sévère sans différence sur CRP, TNF-α, IL-6, HSP90α, Serpin F1, hémopexine, APOA4.