SAMe, méthyl-folate et B12 dans le Covid long : restaurer le pool de méthylation chez le profil hEDS/SAMA/neuroatypie
⚠️ Cet article est délibérément spéculatif. Il prolonge la cartographie mécanistique du profil hEDS/neuroatypie/SAMA (article précédent) vers une rationale nutrithérapeutique : pourquoi ce profil présente un pool SAMe structurellement épuisé, et pourquoi 5-MTHF, hydroxycobalamine et SAMe exogène pourraient en théorie y répondre. Il n'existe aucun RCT sur l'indication combinée dans ce profil. Chaque composant est sourcé séparément. Aucune recommandation de dosage n'est formulée.

① Un pool SAMe structurellement épuisé dans ce profil
Hypothèse étayée — plausibilité mécanistique, absence de mesure directe dans ce profilLe SAMe — S-adénosylméthionine — est le donneur universel de groupements méthyle de l'organisme. Sa synthèse dépend d'une chaîne précise : méthionine exogène (alimentation protéique) → MAT (méthionine adénosyltransférase hépatique) → SAMe. Ce que l'on sait de façon bien établie, c'est que MAT est inhibée par le stress oxydatif, les cytokines pro-inflammatoires et le TNF-α [1].
Dans le profil hEDS/SAMA/neuroatypie exposé à un Covid long, trois mécanismes convergents aggravent structurellement ce déficit :
- Activation mastocytaire chronique (SAMA) — la libération répétée d'histamine, prostaglandines et tryptase entretient un état pro-inflammatoire qui inhibe MAT, réduisant la production de SAMe disponible.
- Dysrégulation immunitaire post-Covid — l'inflammation de bas grade persistante, documentée dans le Covid long, partage exactement les mécanismes d'inhibition de MAT (IL-6, TNF-α) [2].
- Polymorphismes MTHFR (C677T/A1298C) — surreprésentés dans les profils neuroatypiques, ils ralentissent la reméthylation de l'homocystéine en méthionine, limitant le substrat d'entrée du cycle.
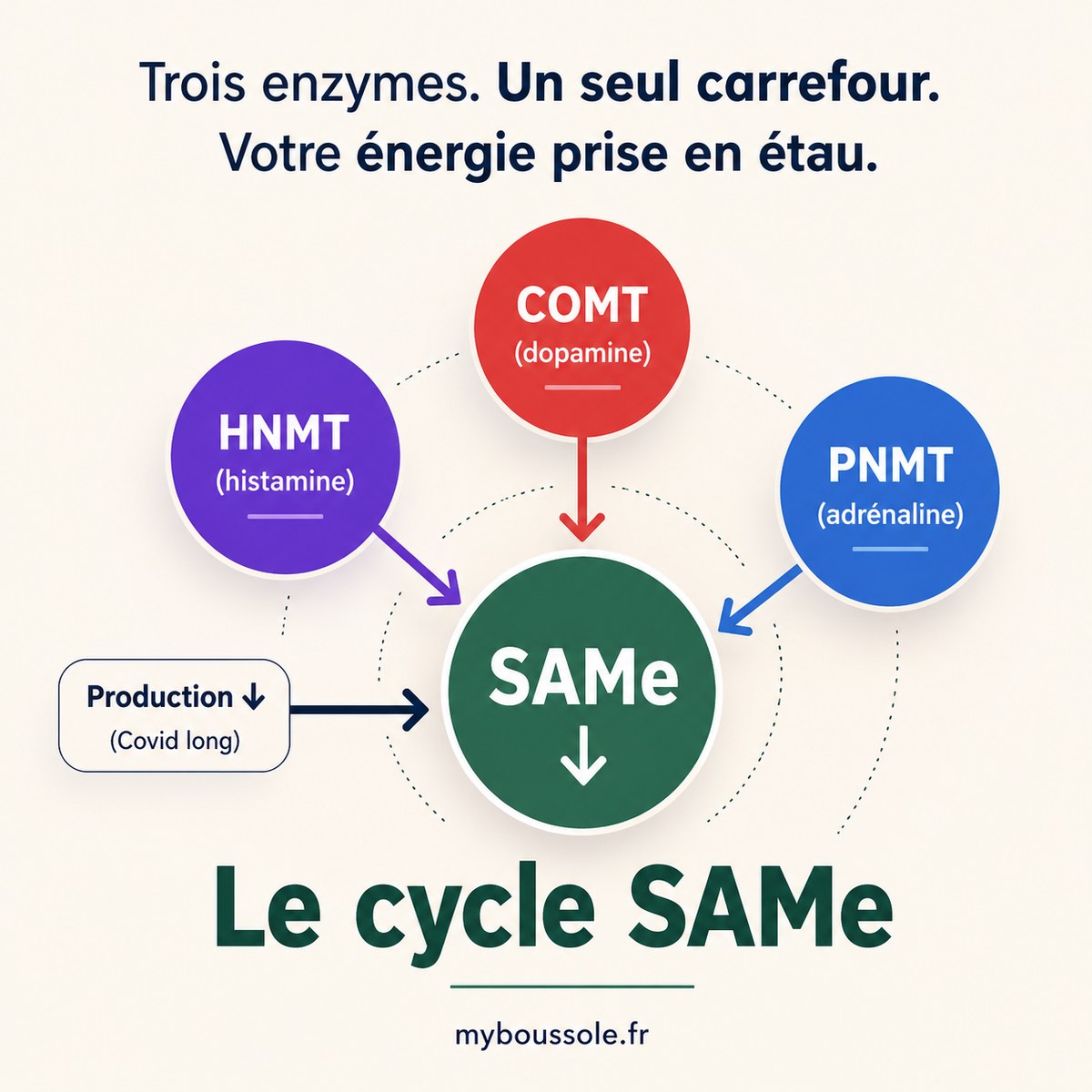
La résultante théorique est un pool SAMe chroniquement bas, exposé à une demande enzymatique élevée. C'est ici que la compétition entre HNMT, COMT et PNMT devient cliniquement déterminante.
Fig. 1 — Les trois enzymes SAMe-dépendantes en compétition simultanée dans le profil hEDS/SAMA/neuroatypie/Covid long. La production hépatique de SAMe est réduite par l'inflammation, pendant que les trois consommateurs enzymatiques tournent à plein régime.
Ce n'est pas un composant qui manque : c'est un carrefour métabolique entier qui est sous tension simultanée de tous les côtés.
② SAMe en compétition : HNMT, COMT, PNMT sous tension simultanée
Hypothèse étayée — chaque enzyme individuellement documentée ; compétition simultanée non mesurée directement dans ce profilL'originalité du profil hEDS/SAMA/neuroatypie est que les trois voies enzymatiques SAMe-dépendantes majeures sont simultanément actives de façon chronique, ce qui ne se produit pas dans la population générale.
- HNMT (histamine N-méthyltransférase) — méthyle l'histamine intracellulaire pour l'inactiver. Dans un SAMA actif, la libération continue d'histamine mastocytaire force HNMT à tourner en régime soutenu, drainant le SAMe à un rythme anormal.
- COMT (catéchol-O-méthyltransférase) — dégrade dopamine, noradrénaline et adrénaline par méthylation. Chez les profils neuroatypiques, le polymorphisme COMT Val158Met est fréquent et ralentit déjà l'enzyme. La compensation paradoxale est une demande accrue de SAMe pour maintenir une dégradation minimale des catécholamines en excès.
- PNMT (phényléthanolamine N-méthyltransférase) — synthétise l'adrénaline par méthylation de la noradrénaline dans la médullaire surrénale. Dans un contexte dysautonomique (POTS, tachycardie posturale), la demande en adrénaline est chroniquement élevée, activant PNMT de façon soutenue.
À titre illustratif, l'inhibition compétitive entre ces voies est conceptuellement analogue à trois organes partageant un même approvisionnement en oxygène — si l'un est en crise, les deux autres sont compromis. La différence ici : les trois sont en crise simultanément.
Fig. 2 — Hiérarchie conceptuelle des consommateurs de SAMe dans le profil hEDS/SAMA/neuroatypie/Covid long. La tension cumulée des trois voies simultanées est l'hypothèse centrale justifiant la stratégie de restauration.
Ce qui rend ce profil cliniquement difficile à traiter par la seule supplémentation en SAMe exogène est précisément cette compétition : apporter du SAMe sans avoir d'abord résolu le goulot de reméthylation revient à remplir un seau percé. D'où l'importance de comprendre le rôle de MTHFR dans la persistance du déficit.
HNMT, COMT et PNMT ne se partagent pas le SAMe — ils se le disputent, et dans ce profil, les trois tirent simultanément.
Consignez vos symptômes SAMA (réactions histaminiques, flush, brouillard mental) et leurs variations dans le temps. L'app Boussole permet de corréler vos ressentis avec vos stratégies nutritionnelles — app.myboussole.fr.
③ Le blocage MTHFR : pourquoi la reméthylation reste insuffisante
Hypothèse étayée — MTHFR C677T associé à une prévalence accrue dans certaines cohortes psychiatriques ; association au Covid aigu documentée, extension au Covid long non établieLa reméthylation de l'homocystéine en méthionine — étape amont indispensable à la production de SAMe — dépend de deux acteurs : la méthionine synthase (MS) catalyse la réaction, et le 5-méthyltétrahydrofolate (5-MTHF) fournit le groupement méthyle. Or, la génération de 5-MTHF à partir des folates alimentaires nécessite l'enzyme MTHFR (méthylènetétrahydrofolate réductase).
Les polymorphismes MTHFR C677T et A1298C réduisent l'activité enzymatique de 30 à 70 % selon le génotype (homozygote vs hétérozygote). Dans certaines cohortes psychiatriques, la prévalence de ces polymorphismes est documentée comme supérieure à la population générale, avec des données mixtes selon les études et les ethnies [3]. Jukic et al. (2023) ont par ailleurs documenté une association entre MTHFR C677T et la sévérité du Covid aigu, avec une accumulation d'homocystéine comme médiateur potentiel [3] — une extension de cette association au Covid long reste une extrapolation non couverte par cette référence.
La conséquence mécanique est claire : même avec un apport alimentaire suffisant en folates, le flux vers le 5-MTHF est ralenti, l'homocystéine s'accumule (risque vasculaire et neurotoxicité), et la reméthylation en méthionine reste insuffisante pour alimenter correctement la production de SAMe par MAT.
Fig. 3 — Le cycle de méthylation avec le goulot MTHFR C677T. Le 5-MTHF contourne directement ce goulot en fournissant la forme active sans nécessiter la conversion enzymatique. La B12 est cofacteur indispensable de la méthionine synthase.
L'implication clinique est importante : suppléer en acide folique standard chez un porteur de MTHFR C677T homozygote n'est pas équivalent à suppléer en 5-MTHF. L'acide folique, non converti, peut même s'accumuler sous forme de folate non métabolisé (UMFA) et exercer des effets compétiteurs sur les récepteurs folate [4]. Cette distinction est particulièrement pertinente pour ce profil où le blocage MTHFR est probablement présent.
Signal de contre-indication à identifier avant introduction : un antécédent d'aggravation neuropsychiatrique (anxiété, insomnie, agitation, ruminations accentuées) sous méthylfolate, méthylcobalamine ou SAMe est un signal évocateur d'un profil Walsh sous-méthylé — phénotype distinct du simple blocage MTHFR, pour lequel les donneurs méthyle peuvent paradoxalement aggraver les symptômes via accumulation de SAH et inhibition secondaire de COMT/HNMT. Ce profil coexiste avec hEDS/neuroatypie. En présence de ce signal, la stratégie décrite ici impose une évaluation spécialisée préalable.
Corriger le déficit en folates avec de l'acide folique chez un porteur MTHFR C677T revient à remplir un entonnoir par le mauvais côté.
④ 5-MTHF et hydroxycobalamine : contourner le goulot enzymatique
Hypothèse étayée — extrapolation mécanistique depuis les données fibromyalgie, psychiatrie, déficits MTHFRSi le blocage MTHFR est le goulot, les deux outils de contournement sont logiquement :
- Le 5-MTHF (lévomeffolate ou L-méthylfolate) — forme biologiquement active des folates, capable de traverser la barrière hématoencéphalique et de servir directement de donneur méthyle à la méthionine synthase sans passer par MTHFR.
- L'hydroxycobalamine — précurseur de toutes les formes actives de B12 (méthylcobalamine, adénosylcobalamine). Cofacteur obligatoire de la méthionine synthase. En son absence, même un apport adéquat en 5-MTHF reste inefficace.
5-MTHF en psychiatrie et neuroatypie
Une méta-analyse de Maruf et al. (2021, Pharmacopsychiatry) a analysé l'effet du L-méthylfolate en augmentation de traitement dans la dépression résistante. Les résultats montrent une réduction significative de la sévérité dépressive comparée au placebo, avec un profil de tolérance favorable [4]. Ces données concernent la dépression, non le Covid long — l'extrapolation à ce profil est spéculative. Dartois et al. (2019) ont décrit des cas pédiatriques de déficit MTHFR traités par méthylfolate avec amélioration des symptômes neuro-psychiatriques [5].
B12 et immunité post-virale
Batista et al. (2022, Nutrition Reviews) ont publié une revue exhaustive du rôle de la B12 dans les infections virales, incluant SARS-CoV-2. Les auteurs documentent le rôle de la B12 dans la régulation de la réponse immunitaire, la synthèse de myéline, et la méthylation de l'ADN viral. Une carence en B12 aggrave la perméabilité de la barrière hématoencéphalique et la neuroinflammation post-virale [8]. Ces données ne prouvent pas l'efficacité de la supplémentation en B12 dans le Covid long spécifiquement, mais elles fondent la rationale mécanistique.
Un point souvent négligé : la B12 sérique standard peut être dans les valeurs normales de laboratoire tout en masquant une carence fonctionnelle. La B12 sérique mesure toutes les formes, actives et inactives. La mesure de l'acide méthylmalonique (AMM) urinaire ou plasmatique est un marqueur fonctionnel plus pertinent de la disponibilité en B12 pour la méthionine synthase — elle reflète directement l'activité de l'adénosylcobalamine, cofacteur de la méthylmalonyl-CoA mutase.
La B12 sérique normale ne garantit pas que la méthionine synthase dispose de son cofacteur en quantité suffisante — seul l'AMM fonctionnel répond à cette question.
⑤ SAMe exogène : données existantes, extrapolation possible ?
Données établies sur composants isolés (dépression, fibromyalgie) — extrapolation à ce profil spéculativeLe SAMe exogène est le seul composant de cette stratégie pour lequel des RCTs de bonne qualité existent — mais dans des indications différentes. Il convient de délimiter précisément ce qui est documenté et ce qui relève de l'extrapolation.
Dans la fibromyalgie
Jacobsen et al. (1991, Scandinavian Journal of Rheumatology) ont conduit un RCT randomisé en double aveugle comparant le SAMe oral à placebo dans la fibromyalgie primaire. Résultat : amélioration significative de la douleur, de la fatigue et de la qualité du sommeil, avec un bon profil de tolérance [1]. Tavoni et al. (1987, Am J Med) ont obtenu des résultats similaires avec le SAMe IV dans un essai plus petit [2]. Ces données établissent que le SAMe réduit certains symptômes de la fibromyalgie — elles ne prouvent pas son efficacité dans le Covid long, ni dans le profil hEDS/SAMA spécifiquement.
Dans la dépression
Une méta-analyse de Sharma et al. (2017, J Clin Psychiatry) et une autre de Peng et al. (2024, J Affect Disord) concluent à une efficacité du SAMe significativement supérieure au placebo dans la dépression unipolaire, avec un effet d'augmentation documenté en association aux antidépresseurs [6,7]. La plausibilité mécanistique repose sur le rôle du SAMe comme précurseur de la dopamine et de la noradrénaline via la reméthylation des catécholamines.
Fig. 4 — Distinction stricte entre données établies par RCTs (fibromyalgie, dépression) et extrapolations spéculatives vers le profil hEDS/SAMA/Covid long. L'absence de RCT sur l'indication combinée est une limite structurelle de cette approche.
Ce que Weinstock et al. (2021) ont observé
Une étude observationnelle de Weinstock et al. (2021) a documenté une prévalence élevée du SAMA dans des populations post-COVID, avec des symptômes chevauchant la fibromyalgie [11]. Si ce chevauchement phénotypique est robuste, la transférabilité des données SAMe fibromyalgie à ce profil devient conceptuellement plus défendable — sans toutefois constituer une preuve d'efficacité.
Les données de fibromyalgie et de dépression sur le SAMe sont solides — mais elles parlent d'autres pathologies. L'extrapolation vers le Covid long est une hypothèse de travail, pas une recommandation clinique.
⑥ Logique de séquençage et vigilances cliniques
Spéculatif — raisonnement mécanistique sans protocole validé dans ce profilLa littérature actuelle hiérarchise ainsi les mécanismes contributeurs du Covid long :
- Dysfonction mitochondriale / déficit ATP — axe le mieux documenté : spectroscopie musculaire ³¹P, VO₂ max réduit à l'effort (Systrom et al.), présent dans la majorité des formes avec fatigue sévère
- Activation immunitaire chronique et inflammation — cytokines élevées (IL-6, TNF-α, IFN-γ) mesurées à 6–12 mois dans plusieurs cohortes ; inhibiteur direct de MAT → réduit secondairement le flux SAMe
- Dysautonomie / dysrégulation SNA — POTS post-Covid documenté chez ~30 % des patients dans les cohortes spécialisées, activation sympathique chronique, élévation de noradrénaline
- Perturbation du cycle méthylation — plausible mécanistiquement, mais sans preuve d'un déficit global en SAMe mesuré directement dans cette population ; les altérations de méthylome observées sont locus-spécifiques et hétérogènes, cohérentes avec une conséquence en aval plutôt qu'une cause en amont
La méthylation est un modulateur secondaire, lui-même perturbé en aval de mécanismes mieux documentés. Cette hiérarchie ne disqualifie pas l'approche nutrithérapeutique décrite — elle la repositionne à sa juste place dans un plan thérapeutique plus large.
Si la rationale mécanistique des sections précédentes est acceptée à titre de cadre de travail, une logique de séquençage en découle naturellement. Elle n'est pas un protocole — c'est une réflexion sur l'ordre d'intervention cohérent avec la mécanique du cycle.
Étape 1 : évaluer le statut fonctionnel avant d'intervenir
Avant toute supplémentation dans ce cluster, les paramètres suivants méritent d'être documentés :
- Homocystéinémie — reflet indirect de l'efficacité de la reméthylation. Une valeur > 12 µmol/L suggère un déficit de reméthylation.
- Acide méthylmalonique (AMM) urinaire ou plasmatique — marqueur fonctionnel de la disponibilité en B12 adénosylcobalamine. Plus sensible que la B12 sérique.
- Génotypage MTHFR C677T/A1298C — si disponible, oriente le choix acide folique vs 5-MTHF.
- Profil clinique COMT — l'histoire personnelle (réponse aux méthyldoneurs, tolérance à la méthylcobalamine) informe sur la vitesse enzymatique COMT sans nécessiter un test génétique.
Étape 2 : corriger les cofacteurs en premier
La logique mécanistique suggère de restaurer d'abord la capacité endogène de reméthylation avant d'introduire un donneur méthyl exogène. Apporter du SAMe exogène sur un cycle dont la reméthylation est bloquée par un déficit en B12 ou en folates risque de déplacer l'embouteillage sans résoudre le goulot. L'ordre proposé sur le plan théorique : B12 active (hydroxycobalamine ou méthylcobalamine selon tolérance COMT) → 5-MTHF → puis SAMe exogène si indication clinique persistante.
Étape 3 : les vigilances non négociables
- SAMe × médicaments sérotoninergiques — contre-indication relative forte, avis médical obligatoire avant toute introduction.
- SAMe × bipolaire — risque documenté d'induction d'un épisode maniaque ou hypomaniaque chez les sujets bipolaires. Prudence extrême dans tous les profils neuroatypiques où cette dimension n'est pas encore clarifiée.
- Suivi homocystéine — une supplémentation en 5-MTHF + B12 efficace doit normaliser l'homocystéine. L'absence de normalisation après 8–12 semaines signale soit un déficit en B6 (voie transsulfuration), soit un problème d'absorption ou de compliance.
- UMFA accumulation (acide folique non métabolisé) — substituer systématiquement le 5-MTHF à l'acide folique dès lors qu'un polymorphisme MTHFR est documenté ou suspecté.
- Profil Walsh sous-méthylé — un antécédent d'aggravation sous 5-MTHF, méthylcobalamine ou SAMe constitue une contre-indication relative à cette stratégie et impose une évaluation biochimique préalable (ratio SAMe/SAH érythrocytaire). Voir : Méthylfolate : pourquoi la “bonne vitamine” aggrave certains profils.
Les profils physiologiques suivants présentent un risque accru d'intolérance aux méthyldoneurs :
- COMT lent (polymorphisme val158Met lent) — la méthylation accrue élève les catécholamines (dopamine, noradrénaline). Chez un profil déjà hypersympathique ou dysautonomique, cette accumulation peut aggraver l'anxiété, l'insomnie et les symptômes POTS. Signal d'arrêt : aggravation des symptômes dysautonomiques dans les 48–72 h suivant l'introduction.
- Profil hypercatécholaminergique — POTS hyperadrénergique, syncopes catécholaminergiques documentées, noradrénaline élevée au tilt test : l'apport de méthyldoneurs actifs (méthylcobalamine, SAMe) augmente le tonus adrénergique et peut précipiter ou aggraver les épisodes dysautonomiques.
- Profil Walsh sous-méthylé (sens biochimique) — paradoxe clinique : ratio SAM/SAH érythrocytaire perturbé avec neurotransmission sérotoninergique basse. L'ajout de méthyldoneurs amplifie l'inhibition COMT → accumulation de catécholamines → aggravation. Contre-indication aux méthyldoneurs directs sans évaluation préalable du ratio SAM/SAH.
En présence d'un de ces profils, l'évaluation par un professionnel expérimenté en biochimie fonctionnelle précède toute introduction de méthyldoneurs.
Restaurer la capacité de reméthylation endogène avant d'ajouter un donneur méthyl exogène, c'est soigner le tuyau avant de monter la pression.
Bilan épistémique — ce que cet article affirme et ce qu'il ne dit pas
À retenir
Le profil hEDS/SAMA/neuroatypie présente une triple compétition enzymatique (HNMT, COMT, PNMT) pour un pool SAMe structurellement réduit par l'inflammation, le polymorphisme MTHFR et l'inhibition de MAT. La rationale d'une restauration séquencée — cofacteurs (5-MTHF + hydroxycobalamine) en premier, SAMe exogène en appoint si indication persistante — est mécanistiquement cohérente et sourcée composant par composant. Elle n'est pas encore validée comme protocole dans ce profil spécifique.
Position épistémique centrale : dans le Covid long, la méthylation n'est pas l'axe causal dominant — elle est un modulateur secondaire, lui-même perturbé en aval de mécanismes mieux documentés (dysfonction mitochondriale, activation immunitaire chronique, dysautonomie). Cette hiérarchie n'invalide pas la stratégie décrite, mais la repositionne : avant d'agir sur la méthylation, adresser l'inflammation de fond et le déficit mitochondrial est probablement plus impactant. La mention explicite du caractère spéculatif de cet article n'est pas une prudence rhétorique : c'est la condition de l'honnêteté scientifique dans un domaine où les patients chroniques sont souvent mal servis par l'excès de certitude.
Questions fréquentes
Ces deux molécules sont des formes réduites et actives du folate, mais elles agissent à des étapes différentes du métabolisme :
- Acide folinique (folinate de calcium, LERDERFOLINE = 5-formyl-THF) : précurseur polyvalent — il alimente à la fois le cycle des nucléotides (synthèse de thymidylate, bases puriques) et peut être converti en 5-MTHF par la MTHFS sans passer par MTHFR. Utilisé en oncologie pour protéger les cellules saines après méthotrexate (rescue leucovorin). Son spectre d'action est plus large : il nourrit la réplication cellulaire ET peut alimenter le cycle méthylation, ce qui en fait le choix de référence en cas de déficit folatique global ou de mucite.
- 5-MTHF (lévomeffolate, méthyl-folate) : forme terminale active du cycle folate — entre directement dans la reméthylation de l'homocystéine en méthionine (via la méthionine synthase + B12), puis en SAMe. Il cible spécifiquement le cycle méthylation/SAMe et contourne le blocage MTHFR, mais n'alimente pas le cycle des nucléotides de manière aussi efficace.
Dans le contexte de cet article (profil MTHFR lent, SAMA, hEDS, Covid long) : l'objectif principal est de restaurer le flux méthylation → SAMe, ce qui positionne le 5-MTHF comme choix de première intention. L'acide folinique (LERDERFOLINE) peut être préféré si vous souhaitez aussi soutenir la synthèse des acides nucléiques (contexte de dysfonction mitochondriale avec ralentissement de la réplication), ou en cas d'intolérance au 5-MTHF. Les deux formes contournent MTHFR — la distinction porte sur la cible prioritaire, pas sur la sécurité d'emploi. Aucun essai comparatif direct dans le Covid long n'est disponible à ce jour.
Suivre vos ressentis dans le temps
L'app Boussole vous permet de corréler vos symptômes SAMA, votre énergie et votre brouillard mental avec vos stratégies nutritionnelles — localement, sans compte obligatoire.
Essayer l'app Boussole →Sources
- Jacobsen S, Danneskiold-Samsøe B, Andersen RB. Oral S-adenosylmethionine in primary fibromyalgia. Double-blind clinical evaluation. Scand J Rheumatol. 1991;20(4):294-302. DOI: 10.3109/03009749109096803 — PMID: 1925418
- Tavoni A, Vitali C, Bombardieri S, Pasero G. Evaluation of S-adenosylmethionine in primary fibromyalgia. A double-blind crossover study. Am J Med. 1987;83(5A):107-10. DOI: 10.1016/0002-9343(87)90571-2 — PMID: 3318438
- Jukic T, Jukic I, Ugrina I, et al. MTHFR C677T variant and COVID-19 severity: a systematic review and meta-analysis. Genes (Basel). 2023;15(1):47. DOI: 10.3390/genes15010047 — PMID: 38138914
- Maruf AA, Partridge S, Shahid M, et al. Folate and related one carbon metabolism nutrients and depression: A systematic review and meta-analysis of randomized controlled trials. Pharmacopsychiatry. 2021;54(6):261-274. DOI: 10.1055/a-1562-4125 — PMID: 34794190
- Dartois LL, Burke JD, Pinto J, Ristic M, Roy A. The use of methylfolate in adolescents with MTHFR mutations and psychiatric illness. J Child Adolesc Psychopharmacol. 2019;29(5):382-385. DOI: 10.1089/cap.2019.0027 — PMID: 31058543
- Sharma A, Gerbarg P, Bottiglieri T, et al. S-Adenosylmethionine (SAMe) for neuropsychiatric disorders: a clinician-oriented review of research. J Clin Psychiatry. 2017;78(6):e656-e667. DOI: 10.4088/JCP.16r11113 — PMID: 28682528
- Peng S, Lu HH, Mao F, et al. SAMe and antidepressants for major depressive disorder: a meta-analysis. J Affect Disord. 2024;346:1-9. DOI: 10.1016/j.jad.2023.11.065 — PMID: 38199136
- Batista KS, Cintra VM, Lucena PA, et al. The role of vitamin B12 in viral infections: a comprehensive review of its relationship with the musculoskeletal and the central nervous system and implications for SARS-CoV-2 infection. Nutr Rev. 2022;80(3):561-578. DOI: 10.1093/nutrit/nuab092 — PMID: 34791425
- Badaeva AV, Bobko EA, Amelin AV, et al. Neuronutritional aspects of fibromyalgia and chronic widespread pain: a review. Nutrients. 2024;16(13):2119. DOI: 10.3390/nu16132119 — PMID: 39042252
- Marx W, Moseley G, Berk M, Jacka F. Nutritional psychiatry: the present state of the evidence. Proc Nutr Soc. 2017;76(4):427-436. DOI: 10.1017/S0029665117002026 — PMID: 28942748
- Weinstock LB, Brook JB, Walters AS, et al. Mast cell activation symptoms are prevalent in Long-COVID. Int J Infect Dis. 2021;112:217-226. DOI: 10.1016/j.ijid.2021.09.043 — PMID: 34563706