Bloc du ganglion stellaire et Covid long : mécanismes, données cliniques et ce qu'il faut vraiment savoir
Une injection d'anesthésique local au niveau du cou — guidée par échographie — pour « réinitialiser » un système nerveux autonome emballé : voilà ce que propose le bloc du ganglion stellaire (BGS). Dans le Covid long et les dysautonomies post-virales, les premières données sont prometteuses — mais elles restent préliminaires, non contrôlées, et la procédure comporte des risques réels. Voici ce que la science sait en 2026, sans raccourci.
Injection d'anesthésique local au ganglion stellaire (C6-C7), sous guidage échographique, pour moduler l'hyperactivité sympathique.
Réduction du NGF → ↓ sprouting sympathique → ↓ noradrénaline centrale. Données animales solides, humaines extrapolées.
Plusieurs cohortes ouvertes (n=10 à 52) rapportent 38–94 % d'amélioration. Aucun RCT publié. Signal fort, preuve faible.
Syndrome de Horner (attendu), dysphonie, pneumothorax rare, injection vasculaire grave. Écho-guidage et centre expert obligatoires.
📖 Glossaire — termes clés de cet article
- BGS (Bloc du Ganglion Stellaire) — injection d'anesthésique local ciblant le ganglion stellaire, relais sympathique cervical.
- Ganglion stellaire — fusion du ganglion cervical inférieur et du 1er ganglion thoracique, situé en C6-C7. Commande sympathique de la tête, du cœur et des membres supérieurs.
- NGF (Nerve Growth Factor) — facteur de croissance nerveux qui favorise la survie et la croissance des neurones sympathiques. Élevé en cas de stress chronique.
- Sprouting sympathique — bourgeonnement pathologique des fibres nerveuses sympathiques sous l'effet du NGF. Amplifie l'hyperactivité adrénergique.
- Noradrénaline (NE) — neurotransmetteur principal du système nerveux sympathique. Responsable de la tachycardie, de la vasoconstriction et de l'hypervigilance.
- COMPASS-31 — score validé d'évaluation des symptômes autonomiques (0-100 ; plus élevé = plus sévère).
- HRV (Heart Rate Variability) — variabilité de la fréquence cardiaque, marqueur indirect du tonus parasympathique. LF : composante basse fréquence (sympathique + parasympathique). HF : haute fréquence (parasympathique).
- PTSD — trouble de stress post-traumatique. Le premier contexte où des RCT ont testé le BGS.
- Syndrome de Horner — ptosis (paupière tombante) + myosis (pupille serrée) + anhidrose (absence de sueur) ipsilatéral. Signe attendu d'un BGS réussi.
① Le ganglion stellaire : anatomie d'un carrefour sympathique
📚 Revue anatomique — Rusu et al. 2025Le ganglion stellaire est un carrefour sympathique cervical, ce qui explique pourquoi son blocage peut avoir des effets larges. Il envoie des signaux vers le cœur, le cerveau, les bras et le système immunitaire. C'est parce qu'il contrôle autant de fonctions qu'un blocage à cet endroit peut avoir des effets aussi variés.
Anatomiquement, ce carrefour sympathique explique la variété des effets attendus et des risques possibles. Le ganglion stellaire (ou ganglion cervico-thoracique) résulte de la fusion du ganglion cervical inférieur et du premier ganglion thoracique chez environ 80 % des individus. Il se situe à la jonction cervico-thoracique, en regard des vertèbres C7-T1, en avant du muscle long du cou et en arrière de l'artère sous-clavière.
Son territoire d'innervation sympathique est large : cœur et vaisseaux coronaires, circulation cérébrale, membres supérieurs, et — via des projections ascendantes — structures limbiques impliquées dans la régulation émotionnelle et la réponse au stress. C'est ce territoire étendu qui explique pourquoi son blocage peut avoir des effets aussi variés : cardiovasculaire, cognitif, émotionnel.
Le guidage échographique (ou fluoroscopique) est désormais le standard de soin : il permet de visualiser le ganglion, d'éviter les structures vasculaires adjacentes (artère carotide, vertébrale, jugulaire) et de déposer l'anesthésique avec précision. Les approches « à l'aveugle » au repérage anatomique seul sont de moins en moins utilisées, en raison d'un taux de complications significativement plus élevé [1].
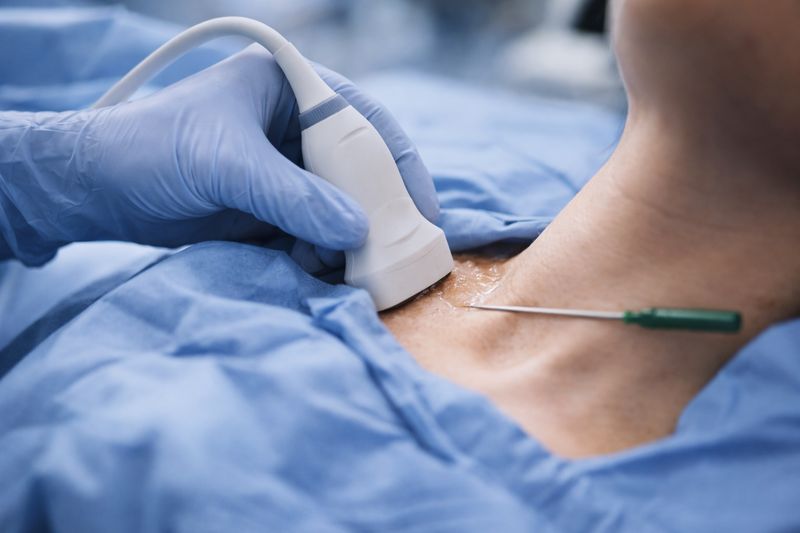
② La cascade NGF : comment l'injection peut « réinitialiser » le système nerveux
🟠 Mécanisme — modèles animaux + extrapolation humaineLe mécanisme proposé est une interruption de l'hyperactivité sympathique, pas une guérison démontrée du Covid long. Lors d'un stress prolongé ou d'une infection, un facteur de croissance nerveux (NGF) augmente et provoque une multiplication anarchique des fibres nerveuses sympathiques. Cela entraîne un excès de noradrénaline dans le corps et le cerveau. L'injection au ganglion stellaire interromprait cette cascade en réduisant le NGF, ce qui expliquerait pourquoi ses effets durent bien au-delà de l'anesthésique.
La cascade NGF/sprouting est une hypothèse mécanistique cohérente, mais extrapolée. Le mécanisme d'action du BGS repose sur une théorie unificatrice proposée par Lipov et ses collaborateurs — et reprise dans plusieurs revues récentes [2, 3]. Elle s'articule en quatre étapes :
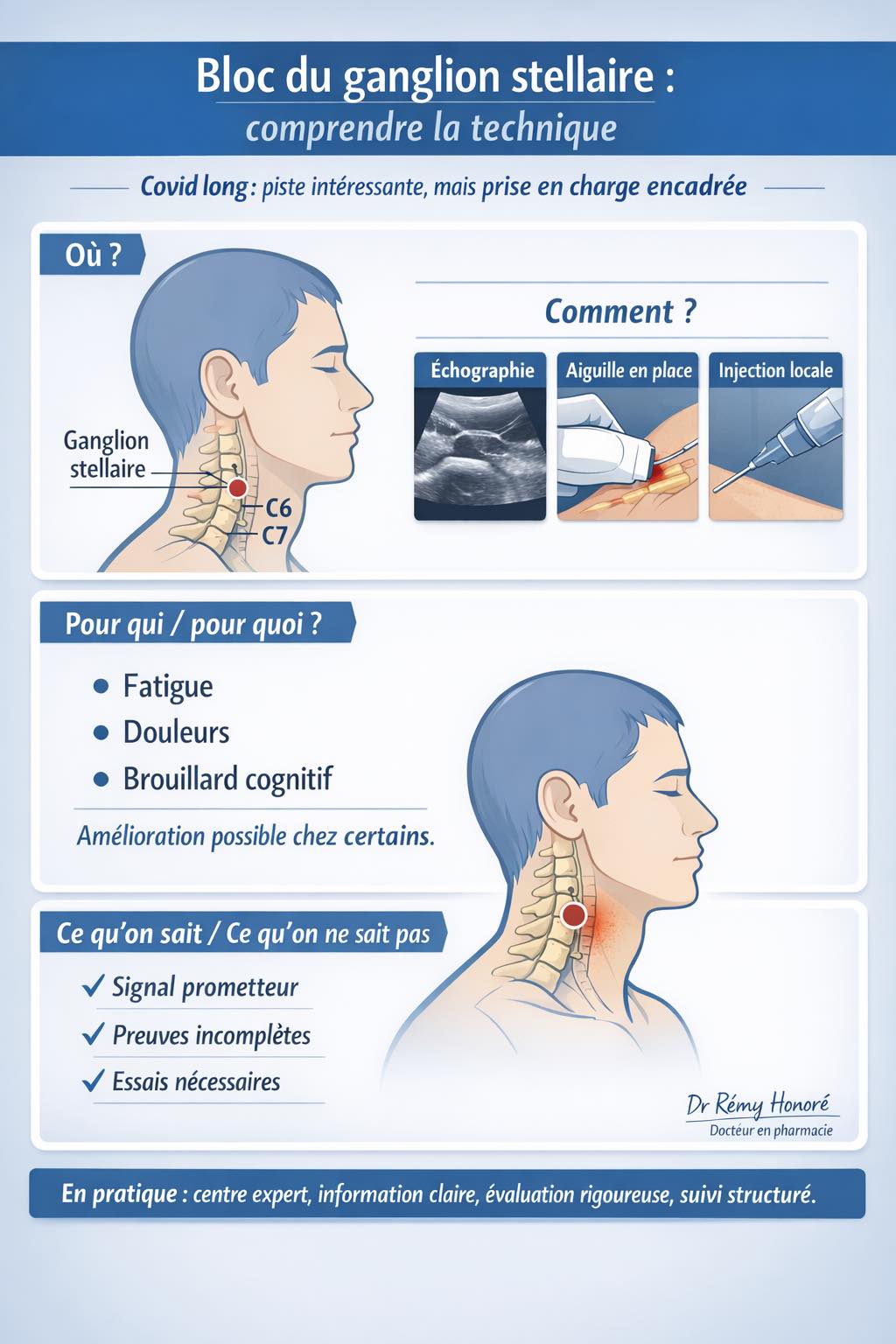
① Stress chronique ou post-viral → ↑ NGF. Le Nerve Growth Factor (facteur de croissance nerveux) augmente en réponse aux cytokines pro-inflammatoires et au stress prolongé. Il agit comme un signal de survie et de croissance pour les neurones sympathiques.
② ↑ NGF → sprouting sympathique. Sous l'effet du NGF, les fibres nerveuses sympathiques bourgeonnent — phénomène documenté dans des modèles animaux cardiaques et dans les contextes de douleur chronique. Ce sprouting amplifie structurellement la transmission adrénergique.
③ Sprouting → ↑ noradrénaline centrale et périphérique. La noradrénaline (NE) — principal neurotransmetteur sympathique — augmente aussi bien dans les organes périphériques que dans des régions cérébrales clés (amygdale, hippocampe), entretenant l'hypervigilance, la tachycardie et l'intolérance orthostatique.
④ BGS → ↓ NGF → inversion de la cascade. L'anesthésique local bloque transitoirement la transmission au niveau du ganglion stellaire. Selon la théorie de Lipov [4], cela suffirait à réduire le NGF local et à inverser progressivement le remodelage sympathique — expliquant pourquoi les effets persistent au-delà de la durée pharmacologique de l'anesthésique (quelques heures).
La durée d'action d'un anesthésique local comme la bupivacaïne ou la ropivacaïne est de 4 à 8 heures au maximum. Si les effets cliniques du BGS persistent des semaines ou des mois, c'est que le mécanisme ne peut pas être uniquement pharmacologique — il implique nécessairement un remodelage neurobiologique. La cascade NGF en est l'explication la plus cohérente avec les données actuelles. Mais — et c'est crucial — les mesures directes du NGF avant/après BGS chez des patients Covid long n'ont pas encore été publiées. Le mécanisme reste une extrapolation du modèle PTSD et des données animales cardiaques.
③ Données cliniques dans le Covid long et la dysautonomie post-virale
🟠 Séries ouvertes · cohortes rétrospectives · aucun RCTDans le Covid long, les données disponibles restent encourageantes mais ouvertes et non contrôlées. Elles se sont accumulées rapidement depuis 2021. Voici l'état des lieux honnête en 2026 — classées par niveau de preuve croissant.
| Étude | Design | n | Résultat principal | Niveau PE |
|---|---|---|---|---|
| Liu & Duricka, 2021 [5] | Case series | 2 | Amélioration fatigue, intolérance orthostatique, anosmie | Case series |
| Pearson et al., 2023 | Cohorte rétro. | 41 | 86 % de réduction des symptômes | Rétrospectif |
| Duricka & Liu, 2025 | Pilote prospectif | 10 | ↓ PEM, OI, brouillard mental ; résolution POTS objectif | Non contrôlé |
| Wang et al., 2025 [6] | Pilote ouvert | 17 (sur 20) | COMPASS-31 −38,4 % (p=0,0016) · douleur −48,4 % · 88,2 % soulagés | Non randomisé |
| Andrassy et al., 2025 [7] | Case report | 2 | Amélioration cognitive et douleur persistante ; résultats mixtes sur la douleur | Case report |
Plusieurs constats transversaux se dégagent de ces études. Les domaines les plus améliorés sont systématiquement le brouillard mental, la fatigue et l'intolérance orthostatique — les trois dimensions les plus invalidantes du Covid long dysautonomique. La durabilité varie de quelques semaines à plusieurs mois. La chronicicité pré-bloc semble influencer les résultats : Andrassy et al. notent que les symptômes présents depuis plus d'un an répondent moins bien [7].
Ces données sont cohérentes et reproductibles d'une équipe à l'autre. Mais toutes partagent les mêmes biais : absence de groupe contrôle, effet placebo non évalué, sélection de patients motivés, et outcomes déclaratifs. Un signal aussi fort dans des études ouvertes peut disparaître en RCT — comme cela s'est partiellement produit dans le PTSD. Aucune de ces études ne permet de conclure à une efficacité établie dans le Covid long.
Si vous envisagez d'explorer le BGS, structurer votre bilan autonomique au préalable est utile : COMPASS-31, intolérance orthostatique, variabilité cardiaque, score de malaise post-effort. Ces données aident le médecin à évaluer votre profil et à suivre l'évolution après la procédure.
Accéder à Boussole gratuitement④ La preuve de concept PTSD : enseignements des essais randomisés
✅ RCT niveau 1B — JAMA Psychiatry 2020Les essais PTSD montrent une preuve de concept, mais ils ne se transfèrent pas automatiquement au Covid long. Le PTSD est à ce jour le seul contexte où des essais randomisés contrôlés ont été publiés sur le BGS. Ces données n'établissent pas l'efficacité du BGS dans le Covid long — mais elles valident la biologie et fournissent un cadre d'évaluation critique.
L'essai Rae Olmsted et al. 2020 (JAMA Psychiatry) est le premier RCT multisite puissamment conduit dans cette indication [8]. Sur 113 militaires en service actif avec PTSD, deux injections droites (semaines 0 et 2) ont produit une réduction du score CAPS-5 de −12,6 points vs −6,1 dans le groupe sham (p = 0,01). L'effet est statistiquement significatif et cliniquement modeste.
À l'opposé, Hanling et al. 2016 (Regional Anesthesia and Pain Medicine) [9] n'ont pas observé de différence significative entre BGS et sham dans une population similaire. Une deuxième injection améliorait les résultats dans les deux groupes — suggérant un fort effet non spécifique de la procédure elle-même.
L'ensemble des RCT PTSD oriente vers un effet réel mais de taille modeste, avec une variabilité importante selon le profil de patient. Les études concordent sur deux points : ① le BGS n'est pas neutre — il y a bien un effet biologique au-delà du placebo ; ② l'identification du bon profil répondeur est le vrai enjeu. Dans le PTSD, les symptômes d'hyperactivation (hypervigilance, trouble du sommeil, sursaut exagéré) répondent mieux que les symptômes d'évitement ou de numbing.
La revue de Springer et al. 2024 (NeuroRehabilitation) [10] résume le niveau de preuve actuel comme « 1B » — c'est-à-dire un RCT de bonne qualité avec un résultat positif, en attendant une méta-analyse robuste. C'est un niveau suffisant pour proposer la procédure en centre expert à des patients sélectionnés, mais pas pour en faire une recommandation générale.
⑤ Effets sur la variabilité cardiaque (HRV) : ce que la science dit vraiment
📊 RCT double aveugle — Keim et al. 2025Le BGS semble surtout réduire le signal sympathique, sans restaurer mécaniquement le tonus vagal. Le bloc du ganglion stellaire réduit bien l'activité du système nerveux de stress, mais il n'augmente pas automatiquement le système de repos (parasympathique). L'amélioration passe par la réduction de l'hyperactivité plutôt que par une restauration de l'équilibre.
L'HRV peut objectiver une baisse du signal sympathique, mais pas prouver une récupération autonome complète. L'HRV (Heart Rate Variability) est un marqueur indirect de l'équilibre sympatho-vagal. En théorie, si le BGS réduit l'activité sympathique, on devrait observer une augmentation du rapport HF/LF et une amélioration de la variabilité globale. La réalité est plus nuancée.
L'étude la plus rigoureuse disponible est le RCT double aveugle de Keim et al. 2025 (Autonomic Neuroscience) [11], conduit sur 12 volontaires sains avec BGS droit écho-guidé. Résultat : aucun changement significatif des indices temporels de l'HRV, mais réduction significative du ratio LF/HF — interprétée comme une inhibition sympathique sélective sans augmentation du tonus vagal. Le nerf vague, adjacent anatomiquement au ganglion stellaire, n'a pas été touché.
Song et al. 2009 (Circulation Journal) [12] ont étudié le BGS bilatéral sur 20 volontaires sains. La conclusion va à contre-courant de l'intuition : le BGS bilatéral réduit la modulation vagale cardiaque (baisse du HF et de la sensibilité baroréflexe). Les auteurs recommandent une prudence particulière chez les patients avec symptômes vagaux à l'injection.
Le BGS réduit bien l'activité sympathique (↓ LF/HF), mais il n'augmente pas mécaniquement le tonus vagal. L'amélioration clinique observée dans les études Covid long passe probablement par la réduction de l'hyperactivité sympathique plutôt que par une restauration du tonus parasympathique. C'est une distinction importante pour interpréter les biomarqueurs de suivi.
⑥ Tolérance et risques : ce qu'il faut connaître avant de consulter
🔴 Procédure invasive — risques réels à connaîtreLe BGS est une procédure invasive du cou : la sécurité dépend du guidage et du cadre expert. Son profil de sécurité est globalement acceptable avec le guidage moderne, mais les complications existent et certaines sont graves.
Le BGS ne peut pas être réalisé en cabinet libéral non équipé. Les conditions minimales sont :
① Guidage échographique — réduit significativement le risque vasculaire et de pneumothorax.
② Monitoring per-procédure — ECG, SpO2, pression artérielle continue.
③ Plateau de réanimation disponible — émulsion lipidique pour toxicité anesthésique systémique, matériel d'intubation.
En dehors de ces conditions, la procédure ne doit pas être réalisée, quel que soit le contexte clinique.
⑦ Qui pourrait en bénéficier ? Profil clinique et lacunes
🟠 Données préliminaires — pas de biomarqueur prédictif validéAucun profil répondeur fiable n'est encore validé, ce qui limite toute promesse individuelle. C'est la question la plus importante — et la moins bien répondue. Aucune des études disponibles n'a identifié de biomarqueur ou de profil clinique permettant de prédire a priori qui bénéficiera du BGS.
Sur la base des profils d'inclusion et des domaines les plus améliorés dans les séries publiées, un profil hypothétique de « bon candidat » se dessine — à titre exploratoire, pas encore validé :
- Dysautonomie objectivée — COMPASS-31 élevé, intolérance orthostatique, tachycardie posturale (POTS)
- Clusters « sickness behavior » — fatigue profonde, brouillard mental, hypervigilance, trouble du sommeil
- Début lié à une infection — Covid long ou ME/CFS post-infectieux de préférence à des formes à longue évolution insidieuse
- Réfractaire aux approches conservatrices — pacing, hygiène posturale, fludrocortisone, bêtabloquants faibles doses essayés et insuffisants
① Mesure du NGF avant/après BGS chez des patients Covid long — le mécanisme central n'a jamais été vérifié directement dans cette population. ② RCT avec groupe sham — indispensable pour dissocier l'effet spécifique de l'effet non spécifique (procédure invasive, attention médicale, espoir). ③ Biomarqueurs prédictifs — cortisol, cytokines, HRV au repos — pour stratifier les patients avant la procédure. ④ Durabilité à 12 mois — aucune donnée contrôlée disponible au-delà de 4–8 semaines.
Ce qui est établi, c'est la réduction de l'hyperactivité sympathique dans des contextes contrôlés. Le BGS réduit bien l'hyperactivité sympathique (↓ LF/HF documenté en RCT double aveugle). La procédure sous guidage échographique est réalisable avec un profil de sécurité acceptable en centre expert. Dans le PTSD, un RCT multisite de qualité (JAMA Psychiatry) montre un effet significatif, modeste, sur les symptômes d'hyperactivation. Les séries Covid long sont cohérentes sur les domaines répondeurs (brouillard mental, fatigue, OI).
Ce qui reste spéculatif, c'est l'efficacité nette dans le Covid long et le profil des répondeurs. La cascade NGF n'a jamais été mesurée directement après BGS chez des patients Covid long. L'absence de RCT dans cette indication interdit toute conclusion sur l'efficacité nette. Le profil de patient répondeur n'est pas identifié. La durabilité à long terme est inconnue. L'effet placebo d'une procédure invasive réalisée dans un contexte d'espoir peut être substantiel — et n'a pas été contrôlé.
Ce qu'il faut retenir
Le BGS est une piste sérieuse mais non prouvée dans le Covid long. Il repose sur une biologie cohérente et documentée — la cascade NGF/sprouting sympathique — et sur des données cliniques préliminaires encourageantes. Les séries publiées montrent des améliorations substantielles de la dysautonomie, du brouillard mental et de la fatigue chez 38 à 94 % des patients traités. C'est un signal qui mérite d'être pris au sérieux.
Mais ces données ne constituent pas encore une preuve. Aucun essai contrôlé randomisé n'a été publié dans le Covid long. La procédure comporte des risques réels qui imposent un centre expert, un guidage échographique et un plateau de réanimation. Elle ne doit pas être réalisée hors de ce cadre, quelle que soit la pression de la demande. La prochaine étape nécessaire est un RCT avec groupe sham dans une population Covid long bien phénotypée.
Un signal prometteur ne dispense pas d'une preuve rigoureuse — surtout quand la procédure est invasive.Questions fréquentes
Qu'est-ce que le bloc du ganglion stellaire ?
Le BGS est-il efficace dans le Covid long ?
Quels sont les risques de la procédure ?
Comment se fait le lien entre le BGS et le NGF ?
Où peut-on se faire réaliser un BGS en France pour le Covid long ?
Quelle spécialité consulter et comment trouver un centre ?
Faut-il réaliser un bilan préalable avant le BGS ?
Combien de temps dure l'effet ? Faut-il répéter les injections ?
Y a-t-il des approches moins invasives qui agissent sur le même mécanisme ?
Quel est le coût du BGS ? Est-il remboursé ?
Un bilan autonomique structuré rend la discussion plus solide avant toute procédure invasive. Boussole vous aide à structurer votre bilan, suivre vos symptômes et préparer vos consultations.
Essayer l'app gratuitementSources
Sources récupérées via PubMed et Consensus. DOIs inclus conformément aux exigences de citation.
- Hughey S et al. (2021). Ultrasound Versus Fluoroscopy for Stellate Ganglion Block: A Cadaveric Study. Pain Medicine, 22(10), 2307–2310. doi:10.1093/pm/pnab182 — PMID : 34051103
- Kirkpatrick K et al. (2023). A Review of Stellate Ganglion Block as an Adjunctive Treatment Modality. Cureus, 15(2), e35174. doi:10.7759/cureus.35174 — PMID : 36949968
- Zhang Z & An M. (2025). The potential role of stellate ganglion block in impacting the central and peripheral systems: a narrative review. Frontiers in Cardiovascular Medicine. doi:10.3389/fcvm.2025.1706435
- Lipov EG et al. (2017). Possible Reversal of PTSD-Related DNA Methylation by Sympathetic Blockade. Journal of Molecular Neuroscience, 62(1), 67–72. doi:10.1007/s12031-017-0911-3 — PMID : 28364364
- Liu LD & Duricka DL. (2021). Stellate ganglion block reduces symptoms of Long COVID: A case series. Journal of Neuroimmunology, 362, 577784. doi:10.1016/j.jneuroim.2021.577784 — PMID : 34922127
- Wang S et al. (2025). Effectiveness of Dual Sympathetic Blocks for Sympathetically Mediated Symptoms in PASC: An Open-Label, Non-randomized Pilot Study. Cureus, 17(3), e81530. doi:10.7759/cureus.81530 — PMID : 40308396
- Andrassy B et al. (2025). Stellate Ganglion Block for Headache Pain and Cognitive Impairment Associated With Long COVID Persisting Over 12 Months: A Case Report. Pain Medicine Case Reports, 9(6), 305–309. PMID : 41135020
- Rae Olmsted KL et al. (2020). Effect of Stellate Ganglion Block Treatment on Posttraumatic Stress Disorder Symptoms: A Randomized Clinical Trial. JAMA Psychiatry, 77(2), 130–138. doi:10.1001/jamapsychiatry.2019.3474 — PMID : 31693083
- Hanling SR et al. (2016). Stellate Ganglion Block for the Treatment of Posttraumatic Stress Disorder: A Randomized, Double-Blind, Controlled Trial. Regional Anesthesia and Pain Medicine, 41(4), 494–500. doi:10.1097/AAP.0000000000000402 — PMID : 27187898
- Springer S et al. (2024). Optimizing clinical outcomes with stellate ganglion block and trauma-informed care: A review article. NeuroRehabilitation, 55(3), 385–396. doi:10.3233/NRE-230236 — PMID : 38995805
- Keim OC et al. (2025). Selective sympathetic action on heart rate variability after ultrasound-guided stellate ganglion block. Autonomic Neuroscience, 263, 103367. doi:10.1016/j.autneu.2025.103367 — PMID : 41352043
- Song JG et al. (2009). Effects of bilateral stellate ganglion block on autonomic cardiovascular regulation. Circulation Journal, 73(10), 1909–1913. doi:10.1253/circj.cj-09-0244 — PMID : 19713654