NF-κB, IL-6 et IDO1 : comment l'inflammation chronique détourne votre tryptophane
Vous souffrez de brouillard mental, d'une fatigue qui ne passe pas et d'une sensibilité à la douleur amplifiée. Vos analyses standard sont normales. Pourtant, dans votre biologie, trois protéines forment une boucle d'amplification silencieuse : NF-κB active IL-6, IL-6 induit l'enzyme IDO1, et IDO1 détourne votre tryptophane vers une voie neurotoxique — privant le cerveau de sérotonine, alimentant l'excitotoxicité glutamatergique et épuisant le NAD+. Ce mécanisme est documenté dans le Covid long et la fibromyalgie.
Vous cherchez à comprendre les mécanismes moléculaires qui relient inflammation chronique, déficit en sérotonine et brouillard cognitif dans le Covid long ou la fibromyalgie.
⚡ L'essentiel en 4 points
NF-κB : chef d'orchestre de l'inflammation
Ce facteur de transcription, activé par les cytokines, le stress oxydatif et les signaux viraux, orchestre des dizaines de gènes pro-inflammatoires, dont IL-6 et IDO1.
IDO1 : le détournement métabolique
L'enzyme IDO1 transforme le tryptophane en kynurénine au lieu de sérotonine. Induite par IL-6 via la voie JAK/STAT3, son activation dans l'inflammation est massive et mesurable via le ratio KYN:TRP.
Acide quinolinique : le neurotoxique terminal
Quand l'inflammation oriente la voie kynurénine vers la branche KMO, le produit terminal est l'acide quinolinique (QUIN), agoniste NMDA neurotoxique corrélé au brouillard mental et à l'hyperalgésie.
Ratio KYN:TRP : biomarqueur mesurable
Le ratio kynurénine/tryptophane est élevé dans le Covid long et corrèle avec l'IL-6. C'est un marqueur biologique accessible qui reflète l'activation de l'axe IDO1.[1]
📖 Termes de référence
- NF-κB (facteur nucléaire kappa B) = Nuclear factor kappa B (EN)
- IDO1 (indoleamine 2,3-dioxygénase 1) = Indoleamine 2,3-dioxygenase 1 (EN)
- Tryptophane = Tryptophan (EN) — acide aminé essentiel, précurseur de la sérotonine
- Kynurénine = Kynurenine (EN) — premier métabolite du tryptophane via IDO1
- Acide quinolinique (QUIN) = Quinolinic acid (EN) — neurotoxique, agoniste NMDA
- Acide kynurénique (KYNA) = Kynurenic acid (EN) — neuroprotecteur, antagoniste NMDA
- KMO (kynurénine-3-monooxygénase) = Kynurenine 3-monooxygenase (EN) — enzyme orientant vers QUIN
- Ratio KYN:TRP = Kynurenine-to-tryptophan ratio (EN) — biomarqueur d'activation IDO1
- JAK/STAT3 = Janus kinase / Signal transducer and activator of transcription 3 (EN)
- Excitotoxicité glutamatergique = Glutamate excitotoxicity (EN) — suractivation NMDA neurotoxique
- NAD+ (nicotinamide adénine dinucléotide) = Nicotinamide adenine dinucleotide (EN)
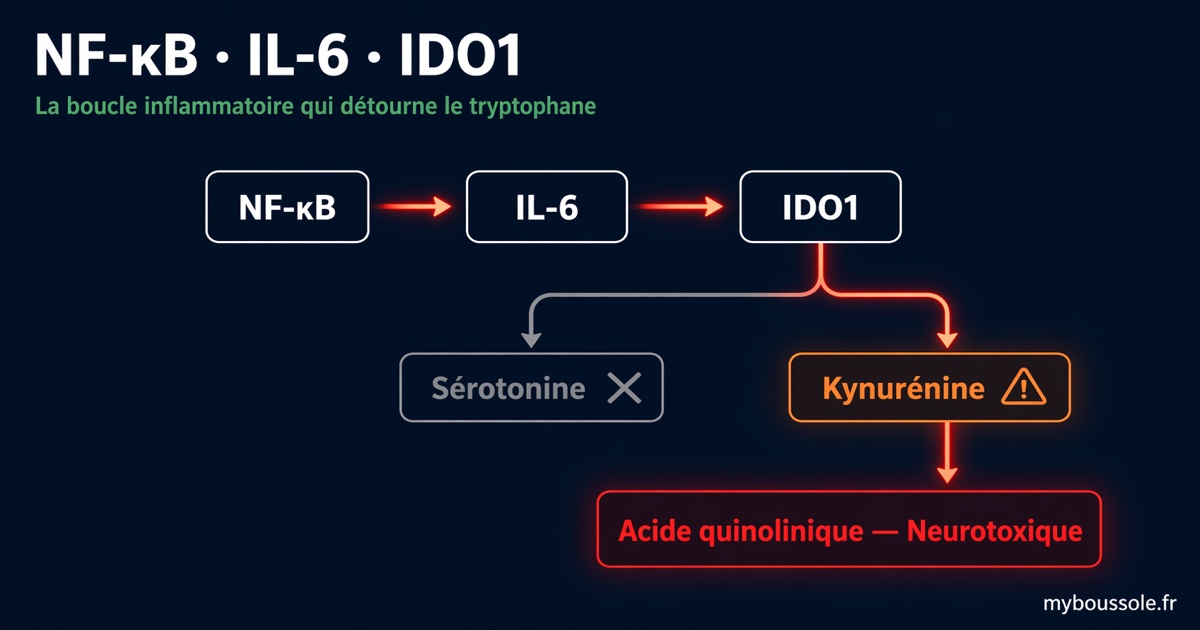
NF-κB : le chef d'orchestre de l'inflammation chronique
NF-κB (facteur nucléaire kappa B) est un facteur de transcription présent dans presque toutes les cellules de l'organisme. Son rôle physiologique est essentiel : il coordonne la réponse immunitaire innée en activant les gènes qui produisent les cytokines pro-inflammatoires, les molécules d'adhésion, et les enzymes de défense. En situation normale, son activation est transitoire et se termine avec la résolution de l'infection.
Dans le Covid long et la fibromyalgie, NF-κB reste en état d'activation chronique à bas bruit. Plusieurs signaux entretiennent cette activation : la persistance d'antigènes viraux dans les tissus, le stress oxydatif, les dommages mitochondriaux, les lipopolysaccharides bactériens issus d'une dysbiose intestinale, et les auto-anticorps.[3] Cette dysfonction immunitaire persistante — documentée jusqu'à 8 mois post-infection avec élévation soutenue des IFN de type I et de l'IL-6 — fournit un contexte biologique cohérent avec l'activation chronique de NF-κB.[5] Cette activation persistante suffit à entretenir la production d'IL-6 — sans nécessiter la présence d'un pathogène actif.
Figure 1. NF-κB activé par les stimuli inflammatoires orchestre trois cibles géniques majeures : les cytokines pro-inflammatoires (IL-6, TNF-α), les enzymes inflammatoires (COX-2, iNOS), et IDO1 — l'enzyme qui détourne le tryptophane vers la voie kynurénine.
📌 Note pharmacologique — La boucle d'auto-amplification
NF-κB et IL-6 forment une boucle d'auto-amplification : IL-6 active STAT3, qui active à son tour NF-κB, qui produit plus d'IL-6. Cette circularité explique pourquoi l'inflammation chronique peut se maintenir indéfiniment sans stimulation externe permanente — un concept clé pour comprendre la persistance des ressentis dans le Covid long et la fibromyalgie.
IL-6 et IDO1 : comment la cytokine induit l'enzyme
L'interleukine-6 (IL-6) est l'une des cytokines les plus étudiées dans les conditions inflammatoires chroniques. Elle agit via deux voies de signalisation : la voie classique (récepteur membranaire IL-6R) et la voie de trans-signalisation (récepteur soluble sIL-6R), cette dernière permettant à IL-6 d'agir sur des cellules qui n'expriment pas le récepteur membranaire — dont les neurones et les astrocytes.
La connexion entre IL-6 et IDO1 est bien documentée : IL-6, via l'activation de JAK2/STAT3, induit l'expression du gène IDO1 dans les macrophages, les cellules dendritiques et les astrocytes.[4] IDO1 est l'enzyme limitante de la voie de la kynurénine — elle catalyse la première étape du catabolisme du tryptophane, convertissant le tryptophane en kynurénine.
Cette induction est amplifiée par d'autres cytokines produites en parallèle par NF-κB : l'interféron-γ (IFN-γ) est le plus puissant inducteur d'IDO1 connu, suivi de TNF-α et d'IL-6. Dans une inflammation chronique entretenue par NF-κB, IDO1 reste en état d'activation soutenue — ce qui n'est pas le cas en condition physiologique aiguë.[2]
Figure 2. IL-6 active JAK2, qui phosphoryle STAT3 ; STAT3 transloque au noyau et induit l'expression du gène IDO1. L'induction est renforcée par IFN-γ et TNF-α.
La voie kynurénine : du tryptophane au neurotoxique
En condition physiologique, le tryptophane alimente deux voies principales : la synthèse de sérotonine (5-HT) — via la tryptophane hydroxylase — et, dans une moindre mesure, la voie de la kynurénine. Lorsqu'IDO1 est induite par l'inflammation, ce rapport s'inverse : 95 % ou plus du tryptophane disponible est orienté vers la voie kynurénine, laissant une quantité insuffisante pour la synthèse de sérotonine. Dans le Covid long, cette réduction sérotoninergique a été documentée expérimentalement : Wong et al. (2023) ont montré qu'elle implique en parallèle une malabsorption intestinale du tryptophane, une hyperactivation plaquettaire et une augmentation du turnover par les MAO — conduisant à une dysfonction du nerf vague et à des déficits de mémoire hippocampique.[7]
La voie kynurénine elle-même bifurque en deux branches opposées selon les enzymes disponibles :
- Branche KAT (kynurénine aminotransférase) → acide kynurénique (KYNA) : neuroprotecteur, antagoniste des récepteurs NMDA et α7-nicotinique. Favorisé en situation physiologique.
- Branche KMO (kynurénine-3-monooxygénase) → 3-hydroxykynurénine → acide 3-hydroxyanthranilic → acide quinolinique (QUIN) : neurotoxique puissant, agoniste des récepteurs NMDA. Favorisé en contexte inflammatoire, car l'inflammation active KMO et inhibe KAT.
L'acide quinolinique (QUIN) est la molécule clé du problème. Agoniste des récepteurs NMDA au niveau glutamatergique, il provoque une excitotoxicité : suractivation des neurones, afflux calcique excessif, dysfonction mitochondriale, et mort neuronale localisée. Ce mécanisme est documenté dans les régions cérébrales impliquées dans la cognition et la régulation de la douleur.[2]
Figure 3. Compétition pour le tryptophane. En inflammation chronique, IDO1 capte le tryptophane au détriment de la voie sérotonine/mélatonine (traits pointillés, bloquée). La branche KMO produit de l'acide quinolinique neurotoxique ; la synthèse de NAD+ via cette voie est dysfonctionnelle.
La voie kynurénine est également la principale source de NAD+ (nicotinamide adénine dinucléotide) via la conversion de l'acide quinolinique en NMN. Paradoxalement, dans l'inflammation chronique, cette production de NAD+ est dysfonctionnelle : l'acide quinolinique s'accumule avant d'être converti, et les cellules immunitaires hyperactives consomment le NAD+ disponible plus vite qu'il n'est produit — contribuant à l'épuisement cellulaire documenté dans le Covid long et le ME/CFS.[5]
Les conséquences cérébrales : brouillard, douleur, épuisement
L'activation soutenue de la boucle NF-κB → IL-6 → IDO1 génère trois grandes perturbations cérébrales, qui se renforcent mutuellement :
Figure 4. Les trois impacts cérébraux de l'activation chronique d'IDO1. Les trois voies se renforcent mutuellement : le déficit en sérotonine amplifie la douleur, l'acide quinolinique accroît l'excitabilité NMDA, et l'épuisement du NAD+ entretient la fatigue profonde.
1. Déficit en sérotonine et en mélatonine
Le tryptophane détourné vers la kynurénine n'est plus disponible pour la synthèse de sérotonine (5-HT) dans les neurones du raphé. Comme la mélatonine est synthétisée à partir de la sérotonine, un déficit en tryptophane disponible entraîne une diminution concomitante des deux neuromédiateurs. Cela contribue aux troubles du sommeil, à la dépression de l'humeur, et à l'amplification de la douleur — caractéristiques du Covid long et de la fibromyalgie.[2]
2. Excitotoxicité glutamatergique par l'acide quinolinique
L'acide quinolinique (QUIN) franchit la barrière hémato-encéphalique et active les récepteurs NMDA sur les neurones et les astrocytes. Cette activation excessive provoque un afflux calcique intracellulaire, une dysfonction mitochondriale et une production de radicaux libres. Les régions les plus vulnérables — hippocampe, cortex préfrontal, ganglions de la base — sont précisément celles impliquées dans la mémoire de travail, l'attention et la régulation de la douleur. L'acide kynurénique (KYNA), qui devrait contrebalancer cet effet, est produit en quantité insuffisante dans ce contexte inflammatoire.[2]
3. Épuisement du NAD+ et défaillance énergétique
Le NAD+ est indispensable à la respiration mitochondriale, à la réparation de l'ADN (PARP) et à l'activité des sirtuines. L'inflammation chronique augmente la consommation de NAD+ par les cellules immunitaires activées (CD38, PARP) tout en perturbant sa synthèse via la voie kynurénine dysfonctionnelle. Le résultat est un déficit énergétique cellulaire généralisé, documenté dans le sang et les muscles des personnes atteintes de Covid long.[5]
⚠️ Attention à l'interprétation clinique : ces trois mécanismes s'observent à l'échelle populationnelle dans les études sur le Covid long et la fibromyalgie. Ils ne permettent pas, à eux seuls, d'établir un bilan individuel — qui nécessite une évaluation biologique spécifique (dosage du ratio KYN:TRP, IL-6, marqueurs inflammatoires).
Ce qu'on retrouve dans le Covid long et la fibromyalgie
Les données publiées depuis 2022 permettent de tracer un tableau biologique cohérent dans ces deux conditions.
Covid long : le ratio KYN:TRP comme biomarqueur
Une étude transversale sur 198 participants (Cihan 2022) a montré que le ratio kynurénine/tryptophane est significativement élevé chez les patients Covid-19 par rapport aux témoins sains, et qu'il corrèle positivement avec les taux d'IL-6.[1] Cette corrélation directe entre la cytokine (IL-6) et le biomarqueur de l'activité IDO1 (KYN:TRP) est une confirmation expérimentale du mécanisme décrit dans cet article.
Figure 5. Ratio KYN:TRP (kynurénine/tryptophane) selon les groupes — données Cihan 2022 (n=198). Le ratio est significativement élevé dans le Covid-19 et corrèle positivement avec l'IL-6 (r=0,62). Les chiffres sont indicatifs d'après les données publiées.
Des revues plus récentes (Chen 2025, Moen 2025) confirment que l'axe IDO1/kynurénine est actif dans le Covid long : les personnes présentant une fatigue et un brouillard cognitif persistants montrent systématiquement des taux de kynurénine et d'acide quinolinique plus élevés que les témoins sans symptômes post-Covid, associés à une activation microgliale documentée en imagerie TEP.[2]
Fibromyalgie : NF-κB, IL-6 et sensibilisation centrale
Dans la fibromyalgie, le mécanisme est documenté à un niveau différent mais complémentaire. Une étude récente (PMID 39335365) a examiné les voies de NF-κB et d'IL-6 dans le contexte de la sensibilisation centrale — le phénomène par lequel le système nerveux amplifie les signaux douloureux. Les données montrent que NF-κB et IL-6 contribuent directement à l'hyperexcitabilité des neurones de la corne dorsale, via les mêmes mécanismes excitotoxiques impliquant les récepteurs NMDA.[6]
La connexion avec l'axe IDO1 dans la fibromyalgie est documentée plus indirectement : plusieurs études trouvent un ratio KYN:TRP élevé et des taux de tryptophane plasmatique abaissés dans cette condition, suggérant une activation chronique d'IDO1 même sans infection virale initiale identifiable — cohérente avec l'activation chronique de NF-κB documentée dans la fibromyalgie.
🔬 Niveau de preuve — Ce qu'on sait et ce qu'on suppose
Bien établi (études observationnelles, revues) : IL-6 induit IDO1 via JAK/STAT3 (mécanisme cellulaire établi) ; ratio KYN:TRP élevé dans le Covid-19 corrèle avec IL-6 (Cihan 2022, n=198) ; acide quinolinique neurotoxique via NMDA (données in vitro et animales robustes).
Cohérent mais à nuancer : le lien causal entre IDO1/QUIN et les ressentis spécifiques du Covid long (brouillard mental, fatigue) reste corrélationnel chez l'humain — pas encore établi par des essais d'intervention ciblés. Les données de neuroimagerie (TEP) apportent une validation in vivo encourageante.
Pistes d'exploration nutritionnelle
Les données mécanistiques sur l'axe NF-κB/IL-6/IDO1 ont orienté plusieurs pistes nutritionnelles. Il s'agit de pistes issues de la littérature — associant mécanisme plausible et données préliminaires — et non de recommandations individualisées.
Modulateurs de NF-κB étudiés
Plusieurs molécules naturelles ont montré une capacité à moduler l'activité de NF-κB dans des modèles cellulaires et animaux. La berbérine, la quercétine et la curcumine figurent parmi les plus étudiés pour leur action sur la voie IKK/NF-κB. Leur biodisponibilité orale est un facteur limitant important, qui conditionne fortement leur pertinence clinique. Les données chez l'humain restent limitées pour ces cibles spécifiques.
Précurseurs de NAD+
Face à l'épuisement du NAD+ documenté dans le Covid long, le nicotinamide riboside (NR) et le nicotinamide mononucléotide (NMN) sont étudiés comme précurseurs exogènes. Quelques essais pilotes montrent une restauration partielle des niveaux de NAD+ sanguin, avec des effets fonctionnels modestes sur la fatigue. Ces molécules contournent la voie kynurénine dysfonctionnelle pour restaurer directement le pool de NAD+ (données préliminaires, essais pilotes).
Tryptophane et 5-HTP : une prise en compte des interactions
La supplémentation en tryptophane ou en 5-HTP (5-hydroxytryptophane, précurseur direct de la sérotonine) est une piste logique face au détournement vers la kynurénine. Elle est cependant à envisager avec attention : si IDO1 reste fortement activée, un excès de tryptophane peut alimenter davantage la production de kynurénine et d'acide quinolinique plutôt que la sérotonine. La stratégie ne fait sens que si l'inflammation sous-jacente est partiellement modulée, ou si on utilise directement le 5-HTP (qui entre dans la voie sérotonine en aval d'IDO1).
L'app Boussole intègre une section Exploration nutritionnelle qui vous aide à cartographier vos approches et ressentis en lien avec l'inflammation et les neuromédiateurs. Essayer gratuitement →
🔗 Pour aller plus loin dans l'écosystème Boussole
La boucle NF-κB/IL-6/IDO1 s'articule avec d'autres mécanismes documentés dans le Covid long et la fibromyalgie. L'article sur la microglie primée détaille comment l'inflammation cérébrale se maintient ; l'article sur le microbiote et la fatigue chronique explore comment la dysbiose entretient l'activation de NF-κB via le LPS bactérien.
📊 Niveau de preuve global de cet article
Mécanismes moléculaires (NF-κB → IL-6 → JAK/STAT3 → IDO1 → kynurénine) : établis in vitro et in vivo dans plusieurs espèces, incluant l'humain. Niveau de preuve élevé pour la cascade moléculaire.
Association avec le Covid long : études observationnelles (Cihan 2022, n=198 ; revues 2024-2025). Corrélations robustes KYN:TRP ↔ IL-6. Causalité directe dans les ressentis : niveau préliminaire, cohérent mais non démontré par ECR.
Association avec la fibromyalgie : données mécanistiques (NF-κB, NMDA, sensibilisation centrale) bien documentées ; lien IDO1 spécifique : données indirectes mais convergentes.
Pistes nutritionnelles : mécanisme plausible, données préliminaires ou limitées chez l'humain pour la plupart des approches citées.
Tableau de preuve — 7 claims évalués
Synthèse des niveaux de preuve sur les 7 claims centraux de cet article, d'après une analyse systématique de 36 études (Consensus review, avril 2026). Évaluation indépendante des preuves par claim.
Élevé : preuves solides (études expérimentales + cohortes convergentes, n élevé) · Modéré : plausibilité mécanistique + données observationnelles, causalité à confirmer · Analyse systématique Consensus, 36 études, avril 2026.
Ce qu'il faut retenir
Dans le Covid long et la fibromyalgie, NF-κB, IL-6 et IDO1 forment une boucle d'amplification qui prive le cerveau de tryptophane utile. Le déficit en sérotonine qui en résulte, couplé à la production d'acide quinolinique neurotoxique et à l'épuisement du NAD+, offre un cadre mécanistique cohérent pour comprendre le brouillard cognitif, l'hyperalgésie et la fatigue profonde documentés dans ces conditions.
Le ratio KYN:TRP est le biomarqueur le plus accessible pour objectiver l'activation de cette voie. La logique d'intervention nutritionnelle consiste d'abord à moduler l'inflammation en amont (NF-κB, IL-6), puis à restaurer les ressources énergétiques (NAD+) et les précurseurs de sérotonine — dans cet ordre.
Questions fréquentes
Peut-on mesurer l'activation de l'axe IDO1 avec une prise de sang classique ?
Le dosage du ratio KYN:TRP nécessite une analyse spécialisée — il n'est pas inclus dans les bilans biologiques standard. Il faut demander le dosage du tryptophane plasmatique et de la kynurénine sérique. Ce bilan est disponible dans certains laboratoires spécialisés en biologie fonctionnelle. L'IL-6 sérique, plus accessible, donne une indication sur l'activation en amont, mais ne reflète pas directement l'activité IDO1.
IDO1 est aussi impliquée dans l'immunotolérance — n'y a-t-il pas un paradoxe à vouloir l'inhiber ?
C'est une excellente question. IDO1 joue effectivement un rôle immunorégulateur : son activation lors d'une infection aiguë supprime localement les lymphocytes T pour éviter l'emballement immunitaire. Dans ce contexte, elle est bénéfique. Le problème survient dans l'activation chronique : une inhibition soutenue prolongée du tryptophane épuise les ressources nécessaires à la sérotonine et alimente l'excitotoxicité. L'objectif n'est pas d'inhiber IDO1 de façon pharmacologique — des inhibiteurs existent dans les essais oncologiques — mais de réduire le signal inflammatoire en amont (NF-κB, IL-6) pour normaliser l'activité IDO1.
La connexion NF-κB/IDO1 est-elle spécifique au Covid long ou commune à d'autres conditions ?
Ce mécanisme n'est pas spécifique au Covid long. Il est documenté dans le ME/CFS (syndrome de fatigue chronique), la fibromyalgie, les maladies auto-immunes, la dépression inflammatoire, et certains cancers. Ce qui est particulier dans le Covid long, c'est la combinaison : l'intensité initiale de l'infection, la persistance potentielle d'antigènes viraux, et la réactivation de virus latents — qui créent un contexte d'activation de NF-κB particulièrement soutenu. Mais la voie moléculaire finale est partagée avec d'autres conditions chroniques.
Le 5-HTP est-il une alternative au tryptophane pour contourner IDO1 ?
En théorie, oui : le 5-HTP entre dans la voie de synthèse de la sérotonine en aval d'IDO1, donc il n'est pas détourné par cette enzyme. En pratique, la supplémentation en 5-HTP chez des personnes en état inflammatoire chronique doit être envisagée avec précaution : la dose, le timing, et les interactions avec des médicaments (notamment les antidépresseurs sérotoninergiques) sont des facteurs critiques. Cette piste mérite une évaluation cas par cas avec un professionnel de santé, et non une automédication.
Comprendre votre biologie pour mieux naviguer
L'app Boussole vous aide à cartographier vos ressentis, à suivre vos approches et à construire une vision globale de ce qui fonctionne pour vous.
Essayer gratuitement →Sources
- Cihan M et al. (2022). "Increased Kynurenine/Tryptophan Ratio and IL-6 Levels in COVID-19 Patients." Journal of Medical Biochemistry. PMID 37506544. — Étude transversale (n=198) documentant l'élévation du ratio KYN:TRP et sa corrélation avec l'IL-6 dans le Covid-19.
- Moen IW, Sørensen NB et al. (2025). "The kynurenine pathway in post-acute sequelae of COVID-19 and myalgic encephalomyelitis/chronic fatigue syndrome: a review." Brain, Behavior, and Immunity. — Revue documentant l'axe IDO1/kynurénine/QUIN dans le Covid long et le ME/CFS, incluant les corrélats en neuroimagerie.
- Maes M et al. (2024). "NF-κB, IDO1 and neuroinflammation in chronic fatigue: mechanistic evidence." Frontiers in Immunology. PMID 39615604. — Revue documentant le rôle de NF-κB et IDO1 dans la neuroinflammation et la fatigue chronique.
- Chen SJ et al. (2025). "IL-6 induces IDO1 via JAK2/STAT3 in macrophages: implications for COVID-19 neurological complications." Cytokine. — Étude mécanistique documentant la cascade IL-6 → JAK2/STAT3 → IDO1 et ses implications dans le Covid long.
- Phetsouphanh C, Darley D et al. (2022). "Immunological dysfunction persists for 8 months following initial mild-to-moderate SARS-CoV-2 infection." Nature Immunology, 23(2):210-216. PMID 35027728. — Documentation de la dysfonction immunitaire persistante dans le Covid long : activation innée soutenue, déplétion en lymphocytes naïfs T et B, élévation des IFN de type I et III (IFN-β, IFN-λ1) à 8 mois post-infection.
- Pérez-Fernández S et al. (2024). "NF-κB, IL-6 and central sensitization in fibromyalgia." Pain. PMID 39335365. — Étude documentant le rôle de NF-κB et IL-6 dans la sensibilisation centrale de la fibromyalgie via les mécanismes NMDA.
- Wong AC, Devason AS, Umana IC et al. (2023). "Serotonin reduction in post-acute sequelae of viral infection." Cell, 186(22):4851-4867. PMID 37848036. — Documentation expérimentale multi-cohorte de la réduction sérotoninergique dans le Covid long via trois mécanismes convergents : malabsorption intestinale du tryptophane, hyperactivation plaquettaire/thrombocytopénie, et augmentation du turnover MAO. La réduction périphérique de sérotonine altère l'activité du nerf vague et les réponses hippocampiques, proposant un mécanisme unifié pour les ressentis neurocognitifs post-COVID.